 Гестаційний пієлонефрит (ГП), або пієлонефрит вагітних – гострий інфекційно-запальний процес з переважаючим ураженням інтерстиціальної тканини, канальцевого апарату і стінок чашково-мискової системи нирки (частіше правої), який вперше розвинувся під час теперішньої вагітності
Гестаційний пієлонефрит (ГП), або пієлонефрит вагітних – гострий інфекційно-запальний процес з переважаючим ураженням інтерстиціальної тканини, канальцевого апарату і стінок чашково-мискової системи нирки (частіше правої), який вперше розвинувся під час теперішньої вагітності
Частота даного захворювання в акушерській практиці складає, за даними різних авторів, 6–10% і, як правило, виникає у вагітних молодого віку в II–III триместрах вагітності (частіше в терміни 20–28 тижнів) [1, 4, 5].
У патогенезі гестаційного пієлонефриту важливе місце належить мембрано-патологічним процесам, зумовленим активацією перекисного окислення ліпідів (ПОЛ) та порушенням стану антиоксидантної системи захисту (АОСЗ) [3]. Тому взаєморівновага в оксидантно-антиоксидантній системі є важливою ланкою в підтриманні гомеостазу взагалі та при патології нирок зокрема і обумовлює включення у комплексне лікування засобів антиоксидантної дії [2, 3, 6].
Перспективним можна вважати застосування фітопрепаратів з високим вмістом біофлавоноїдів та антиоксидантних вітамінів [7, 9, 10]. Високоефективним представником біофлавоноїдів може бути препарат Канефрон® Н компанії «BIONORICA», Німеччина.
Канефрон® Н був вибраний тому, що до його складу входять трава золототисячника, корінь любистку звичайного, листя розмарину.
Ці рослинні компоненти мають комплексний ефект, володіють протизапальною, діуретичною, спазмолітичною і антибактеріальною дією. Однак даних літератури про вплив препарату Канефрон® Н на ПОЛ та АОСЗ у хворих на хронічний пієлонефрит ми не зустрічали.
Метою нашого дослідження було вивчення антиоксидантної активності препарату Канефрон® Н компанії «BIONORICA», Німеччина, при лікуванні хворих на гестаційний пієлонефрит.
Матеріал і методи дослідження
Нами було проведене обстеження та лікування 58 вагітних із гестаційним пієлонефритом. У залежності від обраної схеми лікування, хворі були поділені на дві групи.
До складу групи порівняння (28 осіб) увійшли пацієнтки, які отримували традиційне лікування (відновлення порушеного пасажу сечі, антибіотик з групи цефалоспоринів ІІ або ІІІ покоління, та спазмолітик у середньо-терапевтичних дозах).
Основну групу (30 осіб) склали хворі, яким у комплексне лікування був включений препарат Канефрон® Н. Препарат призначали у дозі 2 драже або 50 крапель 3 рази на день протягом 1 місяця. Середній вік хворих складав 25,8±2,6 років. Групу контролю склали 20 практично здорових вагітних віком від 18 до 40 років.
Стан ПОЛ та активність АОСЗ оцінювали за такими показниками: вміст малонового диальдегіду (МДА), сульфгідрильних груп (СГ) білків і небілкових компонентів плазми крові, рівень активності церулоплазміну та насиченість трансферину залізом.
Отримані дані опрацьовані статистично. За таблицею Ст’юдента–Фішера визначали коефіцієнт достовірності (р). Статистично достовірною вважали різницю при р <0,05.
Результати дослідження та їх обговорення
До початку лікування у хворих на гестаційний пієлонефрит виявлено достовірне посилення процесів ПОЛ (підвищення вмісту МДА на 47,9%) і зниження функціональної здатності АОСЗ: дезадаптація системи церулоплазмін–трансферин (підвищення активності церулоплазміну на 45,4%, зниження насиченості трансферину залізом на 21,3%), зменшення сульфгідрильних груп білків та небілкових компонентів плазми крові: загальних – на 32,1%, залишкових – на 47,2% та білкових – на 29,5% (р<0,05) (табл. 1). 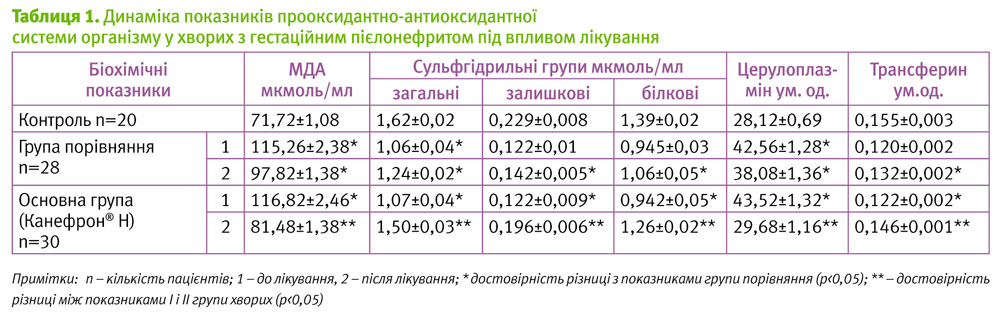
Після проведеного лікування позитивна динаміка клініко-лабораторних проявів захворювання у пацієнтів основної групи, які отримували препарат Канефрон® Н, супроводжувалась суттєвим зменшенням активності процесів ліпопероксидації (зниження вмісту МДА на 33,5% у порівнянні з початковим рівнем) і покращенням функціональної здатності АОСЗ (відновлення майже повної взаєморівноваги у системі церулоплазмін–трансферин, а також підвищення загальних СГ – на 23,2%, залишкових – на 17,9% та білкових – на 23,7% (р<0,05) (табл. 1).
В той же час, у хворих групи порівняння нормалізації показників вільнорадикального окислення ліпідів не відмічено (табл. 1).
Виявлені зміни при дослідженні у хворих на гестаційний пієлонефрит показників вільнорадикального окислення ліпідів – активація процесів ПОЛ і пригнічення АОСЗ – співпадають з даними літератури [2, 3].
Застосування традиційної терапії сприяло зниженню клініко-лабораторних проявів захворювання. Однак залишається високий рівень продуктів пероксидації ліпідів при зниженні антиоксидантного захисту, тобто є умови для подальшого прогресування та хронізації патологічного процесу після припинення лікування.
Застосування у хворих основної групи препарату Канефрон® Н сприяло як нормалізації клініко-лабораторних показників, так і зниженню процесів ПОЛ та відновленню активності АОСЗ.
Висновки
Активація ПОЛ на фоні зниженої активності АОСЗ відіграє важливу роль у процесі хронізації та прогресуванні гестаційного пієлонефриту. Застосування препарату Канефрон® Н у комплексному лікуванні хворих на гестаційний пієлонефрит сприяє скороченню термінів нормалізації клініко-лабораторних показників завдяки відновленню взаєморівноваги між ПОЛ та АОСЗ.
Література
- Аляев Ю. Г., Газимиев М. А., Еникеев Д. В. Современные аспекты диагностики и лечения гестационного пиелонефрита // Урология.– 2008.– №1.– С. 3-6. [1]
- Возіанов О. Ф., Нікуліна Г. Г., Пасєчніков С. П., Бухалов Ю. В. Клініко-лабораторна оцінка активності запального процесу в нирках при гострому пієлонефриті// Лабораторная диагностика. – 1997. – №1. – С. 17-21. [2]
- Литвинець Є. А., Зеляк М. В., Соломчак Д. Б. та інш. Стан перекисного окислення ліпідів і антиоксидантного захисту при патології сечовидільної системи та доцільність використання біофлавоноїдів у комплексному лікуванні//Галицький лікарський вісник. – 2004. – №3. – С. 110-113.
- Потапов В. О., Березницька Г. Г. Гестаційний пієлонефрит//Жіночий лікар. – 2006. – №1. – С. 8-17.
- Серов В. Н., Тютюнник В. Л. Гестационный пиелонефрит: диагностика, профилактика, лечение//Здоровье женщины. – 2010. – №7. – С. 57-60.
- Чекман І. С. Флавоноїди – клініко-фармакологічний аспект // Фітотерапія в Україні. – 2000. – №2. – С. 3-5.
- Anon F. Cranberry juice and urinary tract infections // Harv. Health Lett. – 2005. – Vol. 30. №6. – P.7.
- Howell A. B. Cranberry juice and adhesion of antibiotic-resistant uropathogens // JAMA. – 2002. – Vol. 287. – P. 3082-3083.
- Randomized trial of cranberry-lingo berry juice and Lactobacillus GG drink for the prevention of urinary tract infections in women// T. Kontiokari, K. Sundgvist, M. Nuutinen et al. // BMJ. – 2001. – Vol. 322, №7302. – P. 1571-1573.
- Does cranberry juice have antibacterial activity?/Y. L. Lee, J. Owens, L. Thrupp et al. // JAMA. – 2000. – Vol. 283, № 13. – P. 1691-1693.


коментарів