Низкая эффективность наших усилий в решении проблемы ранних потерь беременности и преждевременных родов (ПР) явилась предпосылкой для научной гипотезы, рассматривающей невынашивание как инструмент естественного отбора. Это находит подтверждение в случаях прекращения развития беременности на предимплатационном и раннем имплантационном периодах вследствие генетических повреждений (гаметопатии и эмбриопатии). Сохранение такой аномальной беременности нежелательно и нецелесообразно, поэтому медикаментозная поддержка беременности до 8 недель в случаях угрозы ее невынашивания отраслевыми регламентирующими документами не предусматривается. Но даже если принять априори, что причиной выкидышей в ранних сроках являются в 50–70% случаев различные летальные хромосомные абберации, то возникает вопрос, а как поступать с остальными 30% беременных с клиническими симптомами угрозы ее прерывания, причины которого могут быть иными (анатомическими, иммунологическими, инфекционными, гормональными и др.)?
В рамках дискуссии по данной проблеме позвольте напомнить о некоторых хорошо известных фактах. Имплантация зародыша в слизистую оболочку матки происходит на 7-е сутки после оплодотворения и с этого момента, по сути, уже начинается биологический процесс формирования плаценты, поэтому последующие 2–3 недели после имплантации определяют дальнейшую судьбу беременности. Нарушение имплантации оплодотворенной яйцеклетки и процесса формирования тесного взаимодействия трофобласта с децидуальной оболочкой матки, вследствие которых происходит поверхностная, субэпителиальная плацентация с анатомической и функциональной неполноценностью межворсинчатого пространства, является основной причиной нарушения трансплацентарного обмена кислорода и питательных субстратов, плацентарной дисфункции, невынашивания, дистресса и задержки роста плода, преэклампсии и антенатальной гибели плода.
Знание этих рисков сформировало ключевую проблему профилактики невынашивания беременности — прицельное наблюдение и оказание помощи беременным групп риска. Однако, попытки создания рациональных систем отбора беременных в группы риска, а также определения перечня самих критериев риска пока не дали желаемого результата в улучшении статистических показателей здоровья и воспроизводства населения, оставляя актуальным вопрос: «Насколько реально влияет формирование групп риска по невынашиванию на популяционные показатели исходы беременности?».
Вопрос далеко не риторический, поскольку общая теория рисков сегодня находится в центре внимания всех сфер деятельности человека и является одной из самых дерзких реформ в сознании человечества: как можно поставить под контроль будущее. Медицинская наука в этом вопросе не исключение и методология оценки риска и профилактические технологии рассматриваются в качестве глобального фактора улучшения здоровья и качества жизни человека. Обычно риск рассматривают как опасность возникновения неблагоприятных последствий, относительно которых неизвестно: наступят они или нет. В акушерстве этот процесс имеет свою особенность, так как контекст подразумевает оценку двойного риска, как для матери, так и ее будущего ребенка. Именно поэтому сегодня в акушерстве возникла насущная проблема изменения стратегии риск-менеджмента, которая должна заключаться не только в формировании групп риска с ограниченными элементами управления рисками в условиях неопределенности, а и в возможности направленного выбора варианта поведения в ситуации, когда имеется возможность оценить предполагаемый результат. Очевидно, что если присутствует возможность оценить предполагаемый результат, то ситуация не такая уж неопределенная.
Нами предлагается в порядке эксперимента ревизия известных на сегодня принципов отбора факторов риска, в частности, невынашивания беременности, и введение такого понятия как «контролируемые» риски.
Под контролируемыми рисками мы подразумеваем риски, которые:
- часто встречаются в популяции;
- легко опознаются (доступная диагностика);
- в арсенале врача имеется возможность несложного их мониторинга,
- имеются проверенные способы их коррекции.
Оценка рисков с вышеуказанных позиций позволяет не только конкретно объективизировать мероприятия по предупреждению их последствий в каждом индивидуальном случае, но и охватить, прежде всего, тот контингент беременных, которые формируют популяционные показатели. Указанный подход имеет и экономический аспект, поскольку можно говорить и о значительном сокращении расходования материальных и человеческих ресурсов на поиск и профилактику неуправляемых, неконтролируемых рисков на современном этапе.
К примеру, сегодня в число факторов рисков невынашивания зачислены анатомические различные причины (аномалии развития, опухоли, ИЦН), некоторые иммунологические причины, связанные с антифосфолипидным синдромом, тромбофилиями, гистосовместимостью, которые не по всем параметрам соответствуют категории контролируемых рисков. Некоторые из перечисленных факторов риска, например, анатомические, имеют невысокую частоту в популяции (1–3%), что объясняет сложность проведения популяционных исследований, имеют нечеткие скрининговые критерии, профилактика их во время беременности имеет ограниченные возможности или невозможна как таковая, а случаи успешного сохранения беременности мало влияют на популяционные статистические показатели. То же касается некоторых иммунологических причин (2–5%) спонтанной преждевременной потери беременности – АФС, тромбофилии, антигены HLA, гистосовместимость. Исключением из данной группы является иммуноконфликтная беременность по резус-фактору и системе АВО, профилактика которой прописана в национальном протоколе.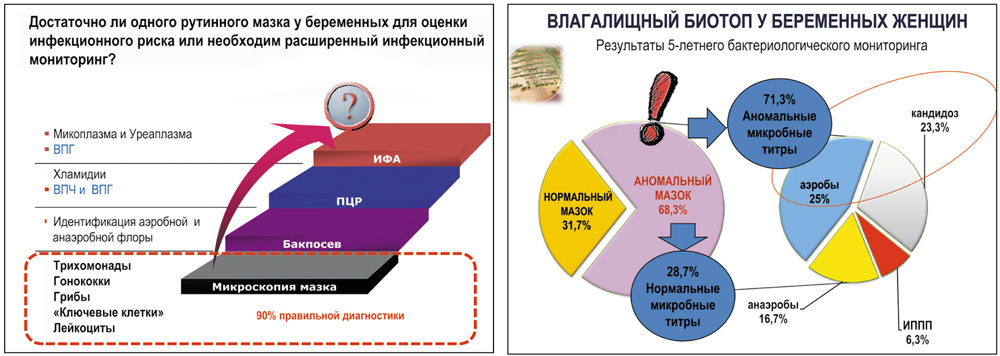
В то же время, воспалительно-инфекционные заболевания наружных женских половых органов широко распространены в популяции беременных и в структуре причин спонтанных потерь беременности, по мнению разных авторов, занимают от 12 до 95%. Доказано, что инфекции, передаваемые половым путем (вагинальный кандидоз, бактериальный вагиноз) являются причинами децидуального эндометрита и хорионамнионита, а значит, непосредственно влияют на процесс имплантации и нарушения развития беременности. Инфекции репродуктивного тракта легко диагностируются, их профилактика и терапия, а также мониторинг результатов этих мероприятий несложны. Поэтому инфекционные факторы риска потери беременности оптимально подходят под понятие контролируемых рисков.
Казалось бы, в вопросе половой инфекции во время беременности нет особых проблем, диагностика и лечение большинства из них прописана соответствующими клиническими протоколами (приказ МОЗ №582). Однако, данный протокол регламентирует деятельность врача в основном у гинекологического контингента пациентов. В отношении же ведения беременных с признаками инфекции репродуктивного тракта возникает сразу несколько принципиальных вопросов.
Как поступать, если у беременной отсутствуют признаки воспаления влагалища, а в мазках из влагалища идентифицированы патогенные или избыточный пул условно-патогенных возбудителей?
- Достаточно ли в качестве скрининга оценки биоценоза влагалища у беременных только бактериоскопического исследования содержимого влагалища (мазка)?
- Как поступать при признаках вагинальной инфекции в сроках до 8 недель беременности, т. е. в период эмбриогенеза и органогенеза?
- Как быть в случае выявления вагинальной инфекции смешанной этиологии, которая у беременных сегодня встречается в 2–3 раза чаще, чем моноинфекция, и лечение которой не прописано клиническими протоколами?
- Нужна ли у беременных профилактическая санация перед родами?
Современные технологии ведения беременности, направленные на снижение акушерской агрессии, сокращение скрининговых и профилактических программ у беременных женщин, большинство этих вопросов просто игнорирует, но ведь от этого они не становятся менее актуальными. Прежде всего, это касается отказа от скрининговых программ по выявлению так называемой группы TORCH-инфекций. Главным аргументов стал тезис, что поскольку мы не можем эффективно лечить эту группу инфекций, нет необходимости и проводить их диагностику.
Можно ли при таком подходе быть уверенным в том, что простое бактериоскопическое исследование мазков ответит на все наши вопросы касательно оценки биоценоза влагалища беременных?
Да, с одной стороны, квалифицированно проведенное бактериоскопическое исследование мазков из влагалища дает 90% диагностики, особенно когда встречаются находки патогенов (гонококк, трихомонада) или «ключевые клетки» как косвенные признаки бактериального вагиноза, но в целом мазок не дает представления о количественном и качественном составе микрофлоры влагалища, а отсутствие повышенного количества лейкоцитов часто свидетельствует не нормоценозе, а о возможном баквагинозе.
Современная наука о микробиоценозе регламентирует его объективную оценку как инструмент профилактики дисбиоза и различных инфекционных осложнений, располагает методами количественной ПЦР-диагностики качественного и количественного состава микробиоты влагалища (Фемофлор-8 и Фемофлор-16), позволяющими выявить степень тяжести дисбиоза от легкого до тяжелого, подходы к лечению и профилактике которых могут быть различными. На наш взгляд, беременная женщина заслуживает такого внимания и нуждается в доступности современных технологий оценки здоровья.
Безусловно, при выраженном дисбиозе лечение должно проводится антибиотиками с антианаэробным эффектом, но следует помнить, что подобная терапия, как и любая антибиотикотерапия, неизбежно приводит с еще большему нарушению биоценоза влагалища и риску развития кандидозной инфекции.
Подобный сценарий исхода терапии предусматривает необходимость использования в схемах лечения бактериального вагиноза и антикандидозной профилактики с использованием антимикотических препаратов.
При легком и умеренном дисбиозе более рационально использовать современные местные пробиотики, которые обладают не только антагонистической активностью к безусловным патогенам и условно-патогенной флоре, но и позволяют быстро восстановить доминантный пул лактобацилл.
Такая градация подходов к терапии бактериального вагиноза дает возможность избежать полипрагмазии, рецидива заболевания и развития кандидоза.
В своей практике в лечении легкого и умеренного дисбиоза влагалища у беременных мы отдаем предпочтение пробиотику Лактожиналь, который содержит штамм лактобактерий (L. casei rhamnosus Lcr 35), выделенных из биотопа влагалища здоровых женщин. Это так называемый «трибиотик», который содержит не только лактобактерии, но и пребиотик (питальную среду), и постбиотик – продукты их жизнедеятельности (молочная кислота) для более быстрого и стойкого восстановления нарушенного баланса микрофлоры.
Эффект Лактожиналя проявляется уже в первые часы его использования и обусловлен быстрым снижением рН благодаря экзогенной донации молочной кислоты, обеспечивающей оптимальные условия для размножения как экзогенным, в составе культуры пробиотика, так и собственным лактобактериям. 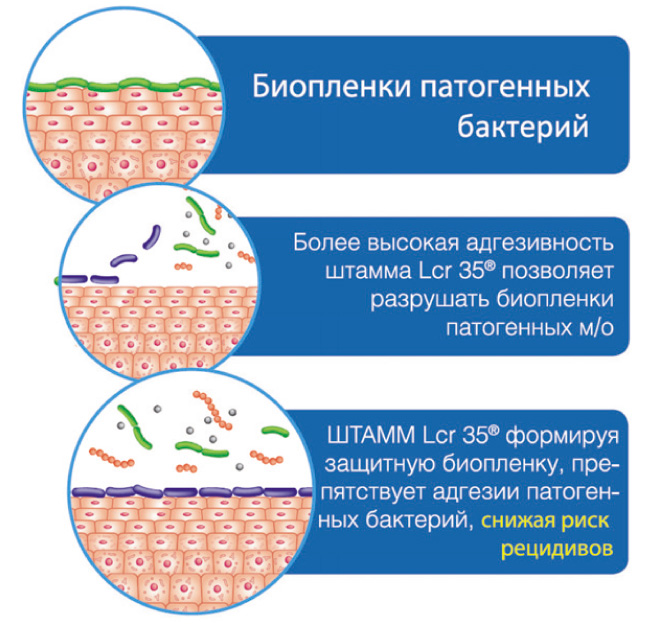
Доказано, что штамм пробиотика Лактожиналь L. casei rhamnosus Lcr 35 обладает высокими адгезивными свойствами и способностью разрушать патогенные микробные биопленки, создавая собственную биопленку из сахаролитических микроорганизмов.
Благодаря этому свойству, пробиотик Лактожиналь способен в течение 6 часов полностью подавить рост главного возбудителя БВ – Gargnerella vaginalis, а в течение 30 часов ингибировать рост Candidа albicans, которая у беременных часто вызывает развитие кандидозного вульвовагинита.
В нашей клинике подтверждена высокая эффективность Лактожиналя в лечении легкого и умеренного бактериального вагиноза у беременных в следующих дозах: 1 капсула 2 раза в день на протяжении 7 дней или 1 капсула 1 раз в день 14 дней.
Следует отметить, что штамм L. casei rhamnosus Lcr 35 в составе пробиотика Лактожиналь обладает природной антибиотикорезистентностью и устойчивостью к противогрибковым препаратам (метронидазол, клиндамицин), что позволяет использовать его параллельно с антибактериальной терапией выраженного дисбиоза и кандидозной инфекции и, таким образом, избежать развития кандидозной суперинфекции и рецидива заболевания благодаря быстрому восстановлению нормального биоценоза после курса терапии.
Не менее распространенным в популяции фактором риска невынашивания беременности, который можно отнести к контролируемым рискам, является дефицит прогестерона, который по данным разных авторов, является причиной выкидышей в 12–30% случаев. Диагностика прогестероновой недостаточности во время беременности не представляет трудности, группы риска женщин, у которых можно предположить ее наличие, подробно изложена в клинических протоколах (приказ МОЗ №624): привычное невынашивание; беременность, наступившая на фоне НЛФ; индуцированная беременность, вылеченное эндокринное бесплодие; беременность, наступившая в результате вспомогательных репродуктивных технологий. 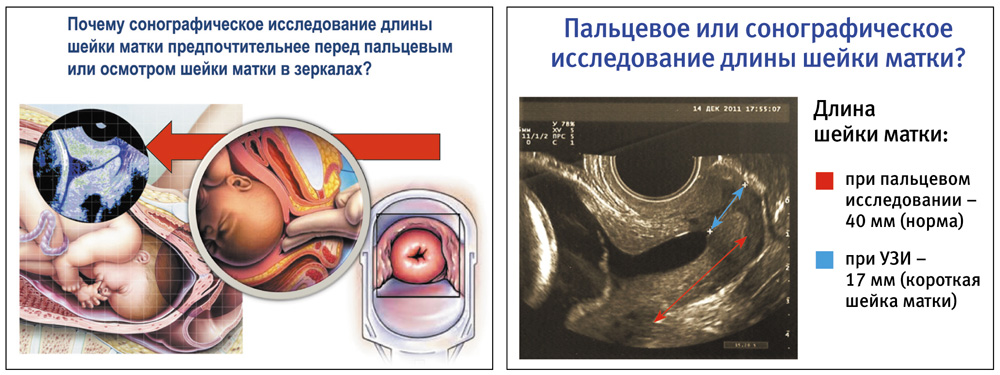
Следует помнить, что до 10 недель беременности источником прогестерона является исключительно желтое тело. При этом его функционирование контролируется эмбриональным ХГЧ, вырабатываемым трофобластом. В более поздние сроки беременности функцию выработки прогестерона берет на себя плацента. Поэтому во время беременности не работают обычные петли обратной связи и регуляция синтеза прогестерона яичниками не находится под контролем гипоталамуса и гипофиза посредством тропных гормонов ФСГ и ЛГ.
В этой связи, при недостаточности прогестерона у беременной донация экзогенного прогестерона является единственным путем его коррекции, а все предостережения относительно угнетения тропных гормонов гипофиза экзогенным прогестероном являются необоснованными.
Интересен также факт, что только биоидентичный прогестерон способен адекватным образом опознаваться клеточной сигнальной системой в организме человека. 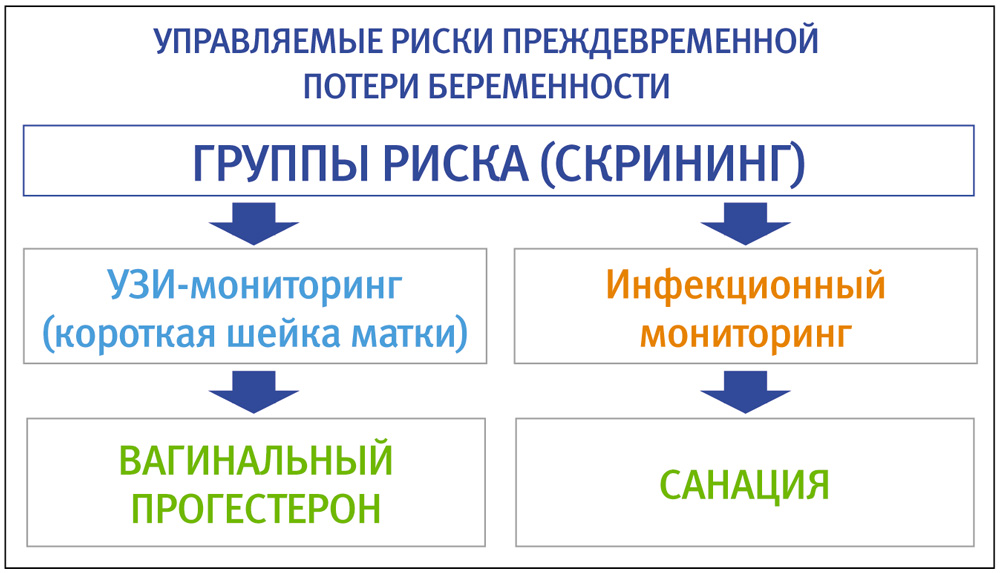
В процессе опознавания и активации системы гормон-рецептор внутриклеточными мессенжерами и сигнальными белковыми молекулами происходит считывание не только количества аминокислот в молекуле прогестерона, но и его уникальной пространственной конфигурации, что в конечном итоге обеспечивает адекватные геномные эффекты, обеспечивающие нормальное развитие беременности.
Одним из проявлений дефицита прогестерона на поздних сроках беременности является синдром бессимптомной короткой шейки матки (КШМ), которая ассоциируется с высоким риском преждевременных родов (Уровень доказательности I-А).
Согласно мнению международных экспертов, сонографическое измерение длины шейки матки трансвагинальным датчиком представляет собой объективный метод оценки риска спонтанного наступления ПР, особенно в случае отсутствия других признаков. При этом за длину шейки матки принимается расстояние от внутреннего до наружного зева по проекции шеечного канала, которая в норме составляет 35–46 мм. Короткой шейкой матки общепринято считается уменьшение ее длины менее 30 мм.
Доказано, что при длине шейки матки менее 30 мм ПР наблюдаются в 10% случаев, а при укорочении менее 20 мм – у каждой третьей беременной с подобной несостоятельностью шейки матки.
Сегодня исследование длины шейки матки для оценки вероятности наступления ПР должно стать основным скрининговым методом, частью стандартной регламентированной сонографической процедуры во II триместре беременных (18–22 недели) на врожденные пороки развития. Почему пальцевое исследование и осмотр шейки матки зеркалах для диагностики короткой шейки матки уступает сонографическому ее исследованию? Суть в том, что укорочение шейки матки идет первоначально за счет раскрытие внутреннего зева и образования так называемой воронки (фанел), образуемой вклиниванием плодного пузыря в просвет шеечного канала, диагностика которых возможна только при трансвагинальном сонографическом исследовании.
Переходя к вопросам лечения невынашивания беременности на ранних сроках и при КШМ, следует отметить, что в настоящее время стандартов терапии этой патологии не существует. Однако накоплен достаточный международный опыт, обобщенный в соответствующих рекомендациях по ведению беременных с КШМ, результаты которого обсуждались не раз как на международных, так и отечественных научно-практических форумах.
Мы в своей практике, следуя этим рекомендациям, используем следующие схемы терапии угрозы НБ: при болях внизу живота натуральный микронизированный прогестерон (Утрожестан) назначается интравагинально в дозе 200–400 мг/сутки. При болях внизу живота, сочетающихся с кровянистыми выделениями, стартовая доза составляет 400 мг/сутки, к ее увеличению до 600 мг обычно прибегают при отсутствии терапевтического эффекта от предыдущей дозы прогестерона. В практической деятельности нам нередко приходится прибегать и к максимальной суточной дозе (800 мг), которая назначается при значительных кровянистых выделениях из половых путей. Можно отметить, что уменьшение размеров ретрохориальных гематом в таких случаях происходит у 2/3 беременных уже через 7–10 дней назначения Утрожестана.
В случае диагностики КШМ в сроках 18–22 недели, Утрожестан профилактически назначаем интравагинально в дозе 200 мг на ночь до 36 недели и 6 дней беременности. В ряде случаев такая терапия является вторым этапом сохраняющей беременность терапии, когда беременным с признаками НЛФ Утрожестан назначался в первом и втором триместрах беременности.
Веские доводы в защиту прогестерона предъявила сама эволюция человека, которая создала и определила именно прогестерон как гормон беременности, а не другое вещество для обеспечения беременности.
Вряд ли нам когда-либо удастся создать искусственно более совершенное средство для сохранения беременности, так не лучше ли рационально использовать то, что уже создано природой и находится в его ареалах. В этом отношении, препарат натурального прогестерона Утрожестан, безусловно, является лидером среди прогестинов и самым назначаемым прогестероном в мире, согласно опросу экспертов в области бесплодия и сохранения беременности.
В резюме хотим отметить, что формирование понятия «контролируемые факторы риска и рациональное управление рисками», в том числе и медикаментозными средствами, стало объективно необходимым условием успешной беременности в современных, порой сложных, условиях жизнеобеспечения, а также ключевым фактором медицинской сферы деятельности, направленной на предотвращение преждевременной потери беременности.


коментариев