
Рак шейки матки — злокачественная опухоль, этиологическим фактором которой являются вирусы папилломы человека (ВПЧ) серотипов № 16, 18, 33, 35 и других [6]. При взаимодействии вируса с эпителиальной клеткой происходит слияние их геномов, что приводит к выработке вирусных белков Е6 и Е7 [14, 16]. Е7 связывается с белковым продуктом гена ретинобластомы (pRb), ингибируя его, что приводит к усилению пролиферации, а Е6 взаимодействует с белком р53, также инактивируя его, что тормозит апоптоз эпителиальной клетки [4].
Ежегодно в мире инвазивным раком шейки матки заболевают около полумиллиона женщин, а 240 тысяч женщин умирают от данного заболевания. Согласно Всемирной базе данных по онкологической заболеваемости — GLOBOCAN [5], частота вновь выявляемых случаев рака шейки матки составляет в Российской Федерации 16,2 на 100 тысяч населения в год, в то же время смертность от данной опухоли составляет 10,1 на 100 тысяч населения в год.
Как уже было сказано выше, белок Е7 вируса папилломы человека 16 и 18 серотипов при своем взаимодействии с продуктом гена ретинобластомы приводит к активации пролиферации. Кроме того, данное событие приводит к увеличению экспрессии гена р16(INK4a), что является биомаркером инициации канцерогенеза в эпителии шейки матки [4, 7, 8, 12]. Было достоверно показано, что экспрессия р16 связана с низкой, умеренной и тяжелой дисплазией (с внутриэпителиальными плоскоклеточными поражениями шейки матки как высокого, так и низкого Grade, LSIL и HSIL соответственно классификации ВОЗ), причем экспрессия р16 не встречалась в плоском эпителии без признаков дисплазии [3, 8, 13]. В то же время, хотя отмечалась четкая корреляция обнаружения ДНК вируса папилломы человека с дисплазиями, имелось также большое количество ВПЧ-позитивных случаев (с эписомальной локализацией ВПЧ), в которых при последующем гистологическом исследовании отсутствовал предрак и рак [8, 13].
Целью исследования было сравнить ПЦР-анализ ВПЧ-инфекции высокого онкогенного риска и иммуноцитохимическое исследование онкомаркера p16ink4a, оценить эффективность жидкостной цитологии относительно традиционной.
Материалы и методы
Всего было исследовано 2754 случая. В данную группу пациентов вошли женщины со средним возрастом 41±2,1 года (от 21 до 62). Была разработана адаптированная транспортная среда для клеточных суспензий. Основу представляла транспортная среда Cytospin Collection Fluid, которая разводилась 1:3 фосфатным буфером, и рН доводился до 7,0. В чистом виде Cytospin Collection Fluid приводит к разрушению клеточных элементов. В адаптированном виде транспортная среда стабильна в течение 6 месяцев при температуре 4–8 °С. Когда в нее вносится клеточный материал, то полученная клеточная суспензия стабильна в течение 10 дней при температуре 4–8 °С, при превышении данного срока иммуноцитохимическое исследование может быть ложноотрицательным. Достаточным объемом адаптированной транспортной среды для проведения исследования является 3 мл, налитых в баночку для сбора мокроты Greiner.
Забор материала осуществлялся цервикальной щеточкой Rovers Cervex-Brush Combi. Данная щеточка позволяет адекватно получить материал из эндоцервикса, экзоцервикса и зоны перехода. После получения материала щеточка интенсивно ополаскивается в баночке с транспортной средой и герметично закрывается.
Полученная клеточная суспензия центрифугируется на цитоцентрифуге Cytospin 4 при среднем ускорении, 800 оборотах в минуту в течение 4-х минут. Для приготовления одного цитопрепарата используется 200 мкл клеточной суспензии, которая вносится при помощи микропипетки Biohit до 1000 мкл в собранную пробирку Cytophanеl (состоящую из цитоклипа, cytophanel, белого фильтра Cytospin и предметного стекла толщиной 1 мм со шлифованным полем для записи). Полученный цитопрепарат высушивается и окрашивается по стандартной методике сокращенного Папаниколау.
Окрашенный препарат подвергается микроскопическому исследованию. Врач-цитолог оценивает цитологическую картину. Если в препарате отсутствует подозрение на дисплазию, то на данном этапе исследование заканчивается, составляется заключение. Если врач выявляет дисплазию или клетки, подозрительные на дисплазию, то выполняется второй этап исследования — иммуноцитохимическое исследование на p16ink4a. Цитологический препарат приготавливается аналогичным образом, после высушивания препарат фиксируется в 95% этиловом спирте в течение 10 минут. После этого осуществляется демаскировка антигенов в цитратном буфере рН6 при температуре 950С в водяной бане в течение 10 минут и остужается при комнатной температуре в течение 20 минут в том же растворе. Далее препарат промывается в трис-буфере в течение 10 минут и обрабатывается раствором для игибирования эндогенной пероксидазы в течение 5 минут. После последующей промывки в трис-буфере осуществляется инкубация первых антител p16ink4a (фирма Santa Cruz, разведение 1:200) в течение 30 минут при температуре 25 °С в условиях водяной бани. Выявление реакции осуществляется при помощи системы визуализации LabVision One в течение 30 минут, в качестве хромогена используется диаминобензидин. Окрашенный препарат оценивается врачом-цитологом. Реакция считалась позитивной, если хотя бы одна диспластическая клетка позитивна на р16ink4a. Оценивается ядерная реакция, ядерная реакция совместно с цитоплазматической. Не учитывается реакция в нормальном метаплазированном эпителии, цервикальном эпителии, атрофически измененном эпителии. Дисплазия считается истинной, если выявляется позитивная реакция на р16ink4a в диспластически измененных клетках.
Результаты жидкостной цитологии сопоставлялись с результатами традиционной. Статистический анализ проводили на персональном компьютере с использованием пакета программ Statistica 6.0. Непараметрические данные анализировались с использованием теста c2. Различия считались статистически достоверными при р<0,05.
Результаты исследования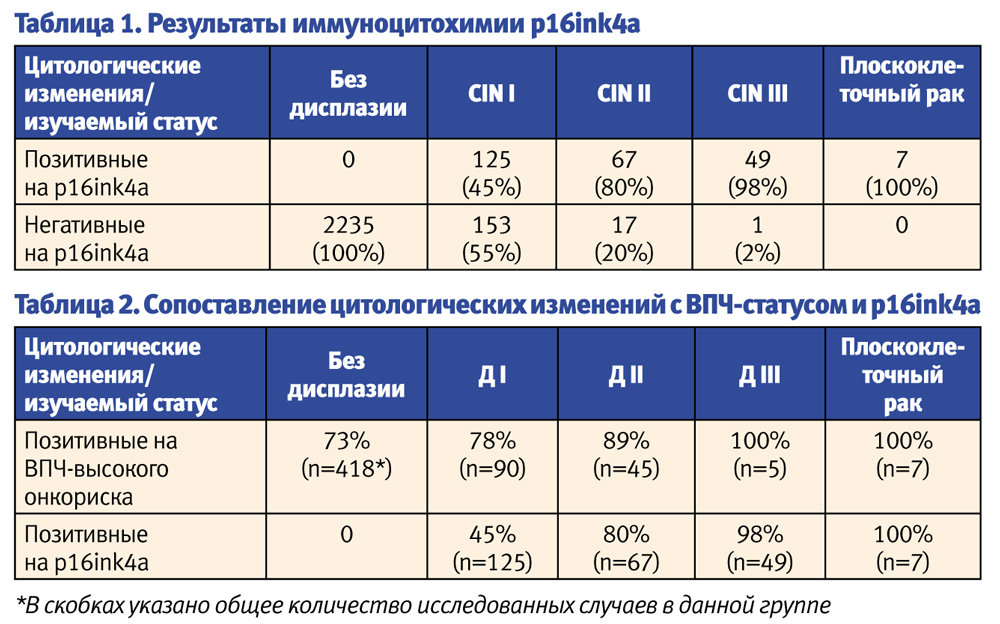
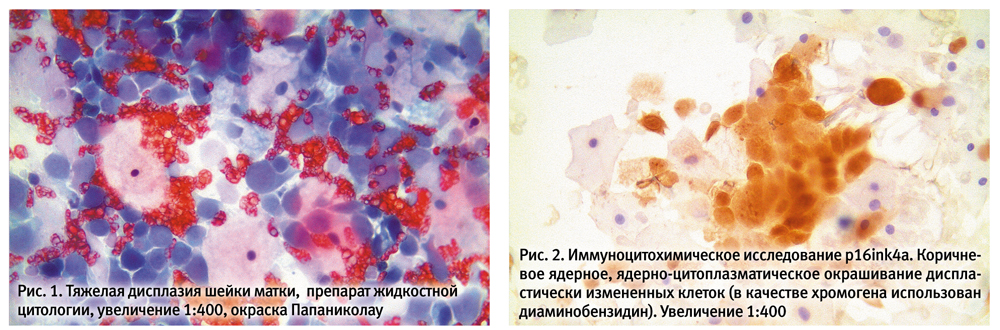
По результатам жидкостной цитологии, из 2754 исследуемых случаев 2235 — не имели дисплазии, в эту группу вошли цитограммы с неизмененным эпителием, воспаления, кандидоза, атрофического кольпита и другие. 278 случаев были с CIN I, 84 пациента — с CIN II, 50 — с CIN III (рис. 1), 7 — с подозрением на плоскоклеточный рак. Иммуноцитохимическое исследование р16 выполнялось в 2754 случаях (100%). Данные ПЦР-исследования ВПЧ высокого онкогенного риска были доступны в 565 случаях (табл. 2).
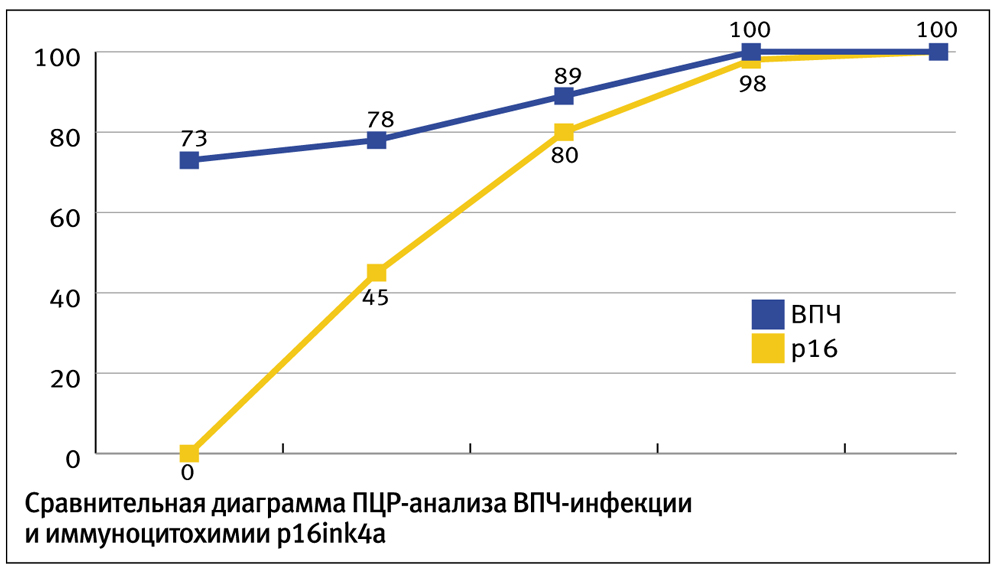
Как видно из таблицы 2, ВПЧ выявлялся в 73% случаев без дисплазии, в 78% случаев — с CIN I, у 89% пациентов — c CIN II, в 100% случаев — c CIN III и плоскоклеточным раком. Таким образом, процент инфицированных ВПЧ в группах c CIN I и CIN II отличается статистически недостоверно (р=0,4835), CIN II и CIN III (p=0,4392).
При анализе экспрессии p16ink4a оказалось, что данный белок не выявлялся в случаях без дисплазии (все пациенты исследовались на наличие р16), у 45% больных с CIN I, у 80% пациентов c CIN II, в 98% случаев CIN III (рис. 2) и в 100% плоскоклеточного рака (табл. 2). Таким образом, процент p16-позитивных наблюдений в группах без дисплазии и CIN I отличается статистически достоверно (р<0,0001), также количество р16-позитивных случаев отличалось статистически достоверно в группах CIN I и CIN II (р<0,001), CIN II и CIN III (p<0,001). В то же время процент p16-позитивных наблюдений в группах CIN III и плоскоклеточного рака отличался статистически недостоверно (р=0,3574).
В рандомизированном мультицентровом исследовании Ronco с соавторами было показано, что мазки, полученные традиционным способом, в 10 раз чаще оказываются неинформативными в сравнении с мазками, полученными методом жидкостной цитологии (10% и 1% соответственно) [15].
В 2002 году жидкостная цитология была рекомендована для использования в скрининге рака шейки матки Американским противораковым обществом (ACS). Жидкостная цитология была также рекомендована для использования Американским обществом кольпоскопии и цервикальной патологии (2006 Consensus Guidelines for the Management of Women with Cervical Cytological Abnormalities) и одобрена для применения FDA. Иммуноцитохимическое исследование цитологических препаратов с использованием метода жидкостной цитологии входит в «Перечень медицинских технологий, разрешенных к применению в медицинской практике по состоянию на 30.01.2009 г.» (регистрационное удостоверение Федеральной службы России по надзору в сфере здравоохранения ФС №2008/082).
Кроме очевидного преимущества самой технологии жидкостной цитологии над традиционной, данное различие связано еще и с тем, что в своём исследовании мы применяли стандартизованный забор материала двумя щеточками Cervex-brush и Cytobrush, в то время как процедура забора материала для традиционной цитологии произвольная. Считается, что использование приспособленных инструментов и средств для забора материала недопустимо, так как это приводит к снижению эффективности скрининга, вплоть до нулевых результатов.
 Как видно из результатов исследования, процент инфицированных ВПЧ возрастал статистически недостоверно в зависимости от увеличения степени CIN. Так, количество инфицированных пациенток с легкой дисплазией превышает число случаев ВПЧ-позитивных без дисплазии всего на 5% (p=0,8631, табл. 1). При сопоставлении последующих групп (CIN I с CIN II и CIN II с CIN III) эта разница оказывается чуть выше (11%), но также является статистически недостоверной (p=0,4835 и р=0,4392 соответственно). Если же мы посмотрим на уровень экспрессии p16 в исследуемых группах без дисплазии c CIN I, CIN I с CIN II, CIN II с CIN III, то процент отличия составляет 16%, 48%, 26% соответственно. Таким образом, наиболее яркое различие в уровне р16 обнаружено между группами CIN I и CIN II (р<0,001), разделяя LSIL и HSIL по классификации Бетезда-2010, что наиболее важно для онкогинекологии. Столь незначительное различие между позитивным статусом ВПЧ-инфекции между группами условно здоровых (по мировой статистике, инфицированность условно здоровых составляет 33%) и CINI может быть связано еще с тем, что ВПЧ-инфекция в нашей стране анализируется при помощи ПЦР-метода. FDA для выявления ВПЧ одобрены только Hybrid Capture® 2 (hc2) и Cervista™ в качестве ко-теста к цитологии (American Society for Colposcopy and Cervical Pathology 2012). ПЦР-тест ВПЧ-инфекции не разрешен из-за большого количества ложноположительных результатов. Кроме того, ПЦР-метод может давать и ложноотрицательные результаты, так в наших исследованиях были выявлены случаи CIN III гистологически верифицированные, в которых при ПЦР-исследовании ВПЧ-инфекция не выявлялась.
Как видно из результатов исследования, процент инфицированных ВПЧ возрастал статистически недостоверно в зависимости от увеличения степени CIN. Так, количество инфицированных пациенток с легкой дисплазией превышает число случаев ВПЧ-позитивных без дисплазии всего на 5% (p=0,8631, табл. 1). При сопоставлении последующих групп (CIN I с CIN II и CIN II с CIN III) эта разница оказывается чуть выше (11%), но также является статистически недостоверной (p=0,4835 и р=0,4392 соответственно). Если же мы посмотрим на уровень экспрессии p16 в исследуемых группах без дисплазии c CIN I, CIN I с CIN II, CIN II с CIN III, то процент отличия составляет 16%, 48%, 26% соответственно. Таким образом, наиболее яркое различие в уровне р16 обнаружено между группами CIN I и CIN II (р<0,001), разделяя LSIL и HSIL по классификации Бетезда-2010, что наиболее важно для онкогинекологии. Столь незначительное различие между позитивным статусом ВПЧ-инфекции между группами условно здоровых (по мировой статистике, инфицированность условно здоровых составляет 33%) и CINI может быть связано еще с тем, что ВПЧ-инфекция в нашей стране анализируется при помощи ПЦР-метода. FDA для выявления ВПЧ одобрены только Hybrid Capture® 2 (hc2) и Cervista™ в качестве ко-теста к цитологии (American Society for Colposcopy and Cervical Pathology 2012). ПЦР-тест ВПЧ-инфекции не разрешен из-за большого количества ложноположительных результатов. Кроме того, ПЦР-метод может давать и ложноотрицательные результаты, так в наших исследованиях были выявлены случаи CIN III гистологически верифицированные, в которых при ПЦР-исследовании ВПЧ-инфекция не выявлялась.
Необходимо особо отметить, что в трех случаях CIN I с позитивной реакцией на p16ink4a при последующем гистологическом исследовании был выявлен рак in situ, а в двух случаях CIN II с позитивной реакцией на p16ink4a обнаружен инвазивный рак.
Таким образом, мы считаем, что жидкостную цитологию в сочетании с иммуноцитохимическим исследованием p16ink4a необходимо внедрять в рутинную практику, так как они являются более эффективными методами в скрининге рака шейки матки в сравнении с традиционной цитологией и ПЦР-анализом ВПЧ высокого онкогенного риска.
Диагностический метод жидкостной цитологии доступен в лаборатории «Синэво Украина» с 01.09.2012. Иммуноцитохимическое исследование p16 планируется производить уже в I квартале 2013 года.
Литература
- Ашрафян Л.А., Харченко Н.В., Огрызкова В.Л., Антонова И. Б. Принципы лечения пре- и микроинвазивного рака шейки матки // Практическая онкология. – 2002. – Том 3. – С. 173-178;17.
- Хансон К.П., Имянитов Е.Н. Современные представления о канцерогенезе рака шейки матки // Практическая онкология – 2002. – Том 3. – С. 145-155;18.
- Bibbo M., Klump W.J., DeCecco J., Kovatish A.J. Procedure for immunocytochemical detection of p16INK4A antigen in thin-layer, liquid-based specimens.// Acta Cytol. – 2002. – V.46 – P. 25-29;15.
- Cripe T.P., Haugen T.H., Turk J.P. et al. Transcriptional regulation of the human papillomavirus-16 E6-E7 promoter by a keratinocyte-dependent enhancer, and by viral E2 trans-activator and repressor gene products: implications for cervical carcinogenesis. // EMBO J. – 1987. – V. 6(12) – P.3745–3753;2.
- GLOBOCANDatabase Jun. 2006. http://www.dep.iarc.fr/globocan/globocan.htm; 3
- Jenison S.A., Yu X.P., Valentine J.M., Galloway D.A. Characterization of human antibody-reactive epitopes encoded by human papillomavirus types 16 and 18. // J Virol. 1991 – V.65(3) – P. 1208–1218;1.
- Klaes R., Froedrich T., Spitkovsky D. et al. Overexpression of p16(INK4A) as a specific marker for dysplastic and neoplastic epithelial cells of the cervix uteri.// Int J Cancer. 2001 – V.92(2) – P.276-84;4.
- Meyer J.L., Hanlon D.W., Andersen B.T. et al. Evaluation of p16INK4a expression in ThinPrep cervical specimens with the CINtec p16INK4a assay: correlation with biopsy follow-up results.// Cancer. – 2007. – V. 111(2). – P. 83-92;20.
- Murphy N., Heffron B., King B. et al. P16INK4A positivity in benign, premalignant and malignant cervical glandular lesions: a potential diagnostic problem.// Virchows Arch. – 2004. – V. 445 – P.610–615;12.
- Nasser S.M., Cibas E.S., Crum C. et al. The significance of the Papanicolaou smear diagnosis of low-grade squamous intraepithelial lesion cannot exclude high-grade squamous intraepithelial lesion.// Cancer. – 2003. – V.99. – P.272-276;16.
- Negri G., Egarter-Vigl E., Kasal A. et al. p16INK4A is a useful marker for the diagnosis of adenocarcinoma of the cervix uteri and its precursors.// Am J Surg Pathol. – 2003. – V. 27 – P.187–193;13.
- Nieh S., Chen S.F., Chu T.Y. et al. Expression of p16 INK4A in Papanicolaou smears containing atypical squamous cells of undetermined significance from the uterine cervix. // Gynecol Oncol. – 2003. – V.91(1) – P.201-8;5.
- Nieh S., Chen S.F., Chu T.Y. et al. Is p16(INK4A) expression more useful than human papillomavirus test to determine the outcome of atypical squamous cells of undetermined significance-categorized Pap smear? A comparative analysis using abnormal cervical smears with follow-up biopsies.// Gynecol Oncol. 2005 – V.99(3) – P.578-84;6.
- Rocco J.W., Sidransky D. p16(MTS-1/CDKN2/INK4a) in cancer progression.// Exp Cell Res. – 2001. – V.264 – P.42-55; 7.
- Ronco G., Cuzick J., Pierotti P. et al. Accuracy of liquid based versus conventional cytology: overall results of new technologies for cervical cancer screening: randomised controlled trial. BMJ. – 2007. – V. 335(7609). – P. 28 – 38;19.
- Sano T., Oyama T., Kashiwabara K., Fukuda T., Nakajima T. Immunohistochemical overexpression of p16 protein associated with intact retinoblastoma protein expression in cervical cancer and cervical intraepithelial neoplasia.// Pathol Int. – 1998. – V.48– P.580-5;8.
- Ylitalo N., Josefsson A., Melbye M. et al. A Prospective Study Showing Long-Term Infection with Human Papillomavirus 16 before the Development of Cervical Carcinoma in situ. // Cancer Research. – 2000. – V. 60 – P. 6027-6032;14.

коментариев