Чим більше ви знаєте про астму, тим менше її боїтесь. Пол Дж. Хенневей «Астма. Помоги себе cам», 1996
Питання бронхіальної астми (БА) все частіше лунає з уст не лише медиків. Суттєвий ріст цієї патології спостерігають як на Україні, так і в світі, а серед пацієнтів все більшу частку складають діти. З позицій клінічної педіатрії стало очевидним, що БА у дітей на даному етапі має ранній дебют і вимагає виважених підходів у лікуванні з огляду на особливості функціонування органів і систем у дитячому віці.
 Однак ми змушені констатувати, що діагностика БА в дитячому віці здебільшого не своєчасна, а тому дитина отримує тривалий час лише симптоматичну терапію, що впливає на формування тяжкості перебігу, знижує якість життя і формує негативний психосоматичний варіант. Залишаються до кінця не вирішеними питання обсягу, складу, тривалості та контролю за ефективністю лікування. БА — важлива медико-соціальна проблема, яка потребує негайного вирішення для покращення якості життя дітей. На сучасному етапі, на жаль, відсутні цільові профілактичні програми для запобігання виникненню алергічних захворювань, в тому числі БА. Досвід останніх років, з моменту прийняття першого протоколу з питань діагностики та лікування БА (1999), який надалі доповнювався та був узгоджений із діючим документом по веденню пацієнтів із БА — GINA (Global Initiative for Asthma), дає підстави робити певні узагальнення. Тобто в даній ситуації ми можемо говорити про вирішені та невирішені проблеми. Серед вирішених слід насамперед виділити прийняття узгодженого визначення бронхіальної астми та класифікації. Трактування БА як хронічного запалення дихальних шляхів, що характеризується варіабельною зворотною бронхообструкцією та гіперреактивністю бронхів, зробило остаточні акценти. У складі БА визначають три основних компоненти: хронічне запалення, здебільшого алергічного ґенезу, бронхообструкція та гіперреактивність бронхів. Саме таке тлумачення БА вимагає цілеспрямованого підходу в лікуванні, що скерований на основну причину — алергічне запалення, а тому є потреба у проведенні базисної терапії.
Однак ми змушені констатувати, що діагностика БА в дитячому віці здебільшого не своєчасна, а тому дитина отримує тривалий час лише симптоматичну терапію, що впливає на формування тяжкості перебігу, знижує якість життя і формує негативний психосоматичний варіант. Залишаються до кінця не вирішеними питання обсягу, складу, тривалості та контролю за ефективністю лікування. БА — важлива медико-соціальна проблема, яка потребує негайного вирішення для покращення якості життя дітей. На сучасному етапі, на жаль, відсутні цільові профілактичні програми для запобігання виникненню алергічних захворювань, в тому числі БА. Досвід останніх років, з моменту прийняття першого протоколу з питань діагностики та лікування БА (1999), який надалі доповнювався та був узгоджений із діючим документом по веденню пацієнтів із БА — GINA (Global Initiative for Asthma), дає підстави робити певні узагальнення. Тобто в даній ситуації ми можемо говорити про вирішені та невирішені проблеми. Серед вирішених слід насамперед виділити прийняття узгодженого визначення бронхіальної астми та класифікації. Трактування БА як хронічного запалення дихальних шляхів, що характеризується варіабельною зворотною бронхообструкцією та гіперреактивністю бронхів, зробило остаточні акценти. У складі БА визначають три основних компоненти: хронічне запалення, здебільшого алергічного ґенезу, бронхообструкція та гіперреактивність бронхів. Саме таке тлумачення БА вимагає цілеспрямованого підходу в лікуванні, що скерований на основну причину — алергічне запалення, а тому є потреба у проведенні базисної терапії.
Наступне, прийняття класифікації, коли тяжкість патології окреслена певним ступенем, є не лише зручним, але й систематизує підходи до визначення тяжкості ядухи за єдиними міжнародними стандартами. Практичні лікарі відчули дієву допомогу з моменту прийняття цієї класифікації, оскільки знялись питання суб’єктивізму у трактуванні тяжкості перебігу БА, а означення чотирьох ступенів тяжкості загострення максимально деталізує особливості конкретного загострення. На даний момент у практиці користуємось класифікацією, яка переглянута та доповнена українськими експертами у 2010 році. Згідно з останнім переглядом, вирізняють БА за:
- етіологією:
алергічна (екзогенна J 45.0)
неалергічна ( ендогенна J 45.1)
змішана ( J 45.8)
- перебігом:
інтермітуючий (І ступінь)
персистуючий легкий (ІІ ступінь)
середньотяжкий (ІІІ ступінь)
тяжкий (ІV ступінь)
Періоди захворювання:
- загострення — прогресуюче зростання ядухи, кашлю, свистячих хрипів, відчуття стискання в грудях;
- контролю — усунення проявів захворювання на тлі базисної терапії БА;
- ремісії — повне усунення симптомів захворювання на фоні відміни базисної терапії.
У випадку діагностики ускладнень БА, серед яких зустрічаються ендокринні (затримка чи відставання в фізичному і статевому розвитку, синдром Іценко-Кушинга, остеопороз, міопатичний синдром, стероїдний діабет), неврологічні розлади , пневмоторакс, ателектази (сегментарний або полісегментарний), пневмосклероз, емфізема (підшкірна, медіастинальна, інтерстиціальна), легеневе серце, слід указати їх у клінічному діагнозі.
Залишаються певні труднощі діагностики БА у дітей різного віку. Увагу лікаря насамперед привертають такі клінічні симптоми: сухі дистанційні свистячі хрипи, кашель (здебільшого вночі і ранковий час), почуття стиснення в грудній клітці, епізоди ядухи з утрудненим видихом. При об’єктивному дослідженні виявлення наступних ознак: задишка експіраторного типу, вимушене положення дитини (ортопноє), дистанційні сухі хрипи, над легенями перкуторно-коробковий звук, аускультативно — ослаблене або жорстке дихання, подовжений видих, сухі свистячі хрипи. Співставляючи наявні клінічні маркери із даними обтяженого алергологічного анамнезу дитини та сімейного, а також результатами додаткових методів дослідження, виставляється діагноз БА.
А тому при підозрі на астму дитині необхідно провести наступні обстеження: рентгенографію органів грудної клітки, загальний аналіз крові (можлива еозинофілія), алерготестування (прік-тести або визначення рівня загального і специфічних IgE методом імуноферментного аналізу), оцінку функції зовнішнього дихання (пікфлоуметрія або спірометрія), пробу з 2-агоністами короткої дії на зворотність бронхообструкції. У дітей перших років життя з метою повної верифікації діагнозу та диференційної діагностики із муковісцидозом — проводиться пілокарпіновий тест. Визначення діагнозу БА вперше потребує ретельної диференційної діагностики. Зокрема, напади нічного кашлю вимагають уточнення його характеру та виключення патології ЛОР-органів (синусити, аденоїдіти, аденоїдні вегетації), гастроезофагального рефлюксу, гострих інфекційно-запальних захворювань дихальних шляхів (ларинготрахеїти, кашлюк, стенозуючий ларинготрахеобронхіт), хронічного стороннього тіла дихальних шляхів, дисфункції гортані, хронічного бронхіту. Симптом свистячого утрудненого дихання з подовженим видихом (wheezing), який раніше вважався патогномонічним для БА, потребує виваженої дифдіагностики, оскільки може спостерігатись і при іншій патології (наприклад при токсокарозі).
Значні труднощі діагностики БА виникають у лікаря, коли пацієнти раннього віку. Водночас діагностика має бути вчасною та виваженою, що підвищує ефективність лікувальних заходів. Експерти GINA запропонували користуватись наступними діагностичними критеріями (що узгоджується із переглядом рекомендацій GINA-2011):
- три і більше епізодів бронхообструкції або wheezing, або крупу, або немотивованого сухого нападоподібного кашлю (особливо в нічний час) протягом року або один типовий напад ядухи;
- обтяжена спадковість з алергії (особливо по материнській лінії);
- підвищений рівень загального та специфічних IgE в крові;
- висока ефективність пробної бронхолітичної та превентивної базисної терапії.
Вищенаведені рекомендації допомагають покращити своєчасність виявлення БА у дітей перших років життя. Слід зауважити, що у лікаря підозра на БА в дитини раннього віку може виникнути за таких обставин: епізоди свистячого дихання з частотою більше 1 разу на місяць; поява нападу кашлю або wheezing на фоні підвищеної (емоційної та рухової) активності; поява нападів кашлю переважно вночі, за умови відсутності ознак гострої респіраторної інфекції; відсутність сезонності wheezing; персистенція симптомів у дітей старше 3 років; зв’язок симптомів БА (кашель, свистяче дихання) із контактом з тваринами, пилюкою, цвітінням рослин, фізичним навантаженням, тютюнопалінням тощо. Обізнаність та настороженість педіатра на предмет БА надалі потребує комплексного обстеження дитини, консультації алерголога та узгодженого лікування.
При первинному визначенні діагнозу БА необхідне проведення ретельної диференційної діагностики
Основними принципами лікування БА вважають:
- визначення факторів ризику захворювання та усунення контакту з ними (елімінаційні заходи);
- оцінка, досягнення і моніторинг рівня контролю БА;
- лікування загострення;
- розвиток партнерських відносин у ланцюгу «пацієнт — сім’я — лікар».
Однак з позицій клінічного досвіду важливо, щоб лікар чітко формулював згідно з цими принципами завдання та конкретизував шляхи його виконання. А тому слід розуміти, що у веденні хворого з БА є певні етапи, які мають конкретні цілі. Етапність лікувальних заходів передбачає: ліквідацію загострення, елімінаційні заходи, проведення базисної терапії, тривалої бронходилятаційної (за показаннями), досягнення контролю над перебігом БА; підвищення якості життя дитини. Чітке формулювання мети лікувальних заходів має бути узгодженим із обсягом, складом та тривалістю фармакотерапії; що значною мірою на даний час потребує суттєвого перегляду.
 Торкаючись питання лікування, очевидною є необхідність обґрунтувати потребу в госпіталізації дитини. Приводом до госпіталізації є: важке загострення ядухи, відсутність ефекту від розпочатої терапії впродовж 2–6 годин; вперше діагностована БА; проведення алергенспецифічної імунотерапії. Окрім цього, в стаціонар необхідно скерувати дітей із високим ризиком смерті від БА: пацієнти, що мають залежність від β2-агоністів короткої дії (часте вживання, при якому одного інгалятора не вистачає на місяць); в анамнезі є дані про інтубацію або штучну вентиляцію легень; наявність загострень, що потребували госпіталізації протягом останнього року; пацієнтів, які отримують контролюючі препарати — системні глюкокортикостероїди, або нещодавно завершили їх прийом; діти, що виховуються в соціально-неблагополучних сім’ях, не отримують адекватної терапії, не дотримуються лікарських рекомендацій. За таких обставин перевага надається спеціалізованим (алергологічним) відділенням. Узагальнюючи, слід наголосити на диференційованій госпіталізації дітей із БА в дитячі стаціонари, щоб уникати контакту з пацієнтами, хворими на гострі бронхолегеневі захворювання, з чисельними вогнищами хронічної інфекції, і тим самим звести нанівець ймовірність контамінації слизових оболонок дихальних шляхів інфекційними чинниками.
Торкаючись питання лікування, очевидною є необхідність обґрунтувати потребу в госпіталізації дитини. Приводом до госпіталізації є: важке загострення ядухи, відсутність ефекту від розпочатої терапії впродовж 2–6 годин; вперше діагностована БА; проведення алергенспецифічної імунотерапії. Окрім цього, в стаціонар необхідно скерувати дітей із високим ризиком смерті від БА: пацієнти, що мають залежність від β2-агоністів короткої дії (часте вживання, при якому одного інгалятора не вистачає на місяць); в анамнезі є дані про інтубацію або штучну вентиляцію легень; наявність загострень, що потребували госпіталізації протягом останнього року; пацієнтів, які отримують контролюючі препарати — системні глюкокортикостероїди, або нещодавно завершили їх прийом; діти, що виховуються в соціально-неблагополучних сім’ях, не отримують адекватної терапії, не дотримуються лікарських рекомендацій. За таких обставин перевага надається спеціалізованим (алергологічним) відділенням. Узагальнюючи, слід наголосити на диференційованій госпіталізації дітей із БА в дитячі стаціонари, щоб уникати контакту з пацієнтами, хворими на гострі бронхолегеневі захворювання, з чисельними вогнищами хронічної інфекції, і тим самим звести нанівець ймовірність контамінації слизових оболонок дихальних шляхів інфекційними чинниками.
Терапія загострення (або симптоматична) передбачає використання інгаляційних форм бронхолітиків швидкої дії. Алгоритм надання невідкладної допомоги полягає у потребі:
- оцінити стан тяжкості дитини (частота дихання і серцевих скорочень, вимірювання пікової об’ємної швидкості видиху (ПОШв), об’єктивне обстеження);
- стартова терапія розпочинається інгалюванням β2-агоністів короткої дії (сальбутамолу) з інтервалом у 20 хвилин протягом 1 години, із використанням спейсера або небулайзера;
- оцінка відповіді на стартову терапію;
- у разі доброї відповіді, тобто легкого ступеня загострення (ПОШв >80% від належного або найкращого індивідуального показника дитини; ефект утримується впродовж 3–4 годин), наступні 24–48 годин продовжуємо інгаляції β2-агоністів короткої дії кожні 3–4 години.
Особливу увагу батьків необхідно звернути на важливість повторних інгаляцій β2-агоністів протягом 1–2 діб, а також обов’язкового огляду лікаря за рекомендаціями. Здебільшого батьки, здобувши навики з надання невідкладної допомоги, обмежуються першими необхідними інгаляціями, а далі бачать полегшення стану дитини, зникнення «свисту в грудях» і припиняють терапію. В цьому криється чи не найголовніша тактична помилка. Батькам важливо пояснювати, що «візуальне» полегшення самопочуття їх дитини не асоціюється із повним купуванням загострення. Купування бронхоспазму має бути остаточним, а зняття набряку та явищ гіперсекреції бронхіальних залоз — завершитись відходженням харкотиння слизистого характеру. А тому важливим є правильне застосування засобів невідкладної допомоги та обов’язковий огляд лікаря. Загострення легкого та середньотяжкого ступенів, за умови доброї відповіді на бронхолітичну терапію, ведуть в амбулаторних умовах під наглядом лікаря-педіатра або дитячого алерголога.
Будь-яке поєднання БА та іншої соматичної патології зумовлює перегляд та корекцію протокольної терапії
У випадку неповної відповіді на стартову терапію лікувальні заходи доповнюють інгаляційними холінолітиками (іпратропіуму бромід). Їх ефективність висока при підгострому типі бронхообструкції, що зумовлений переважанням набряку слизової оболонки та гіперсекрецією. Некупований в амбулаторних умовах приступ БА є приводом для госпіталізації хворого.
Наступним етапом є проведення базисної терапії для подолання активності хронічного алергічного запалення та досягнення контролю над БА. Базисна терапія рекомендована пацієнтам із персистуючим перебігом ядухи та здійснюється інгаляційними глюкокортикостероїдами (ІГКС) впродовж 6 місяців. Дозування ІГКС залежить від ступеня тяжкості БА та віку дитини (по будесоніду):
- до 12 років (ДД): легкий перебіг — 100–200 мкг; середньотяжкий — 200–400 мкг; тяжкий — більше 400 мкг.
- після 12 років (ДД): легкий перебіг — 200–400 мкг; середньотяжкий — 400–800 мкг; тяжкий — 800–1600 мкг.
Базисними препаратами в разі інтермітуючого (вірусіндукованої обструкції) та легкого персистуючого перебігу БА можуть бути застосовані антилейкотрієнові препарати (монтелукаст, зафірлукаст). Тривалість такого лікування до 1 року. Окрім того, з метою купування хронічного алергічного процесу у дітей із легким персистуючим та інтермітуючим перебігом БА використовують кромоглікат або недокроміл натрію. Звичайно, їх ефективність нижча, аніж дія низьких доз ІГКС, однак вища безпечність. Достатньо велика кількість клінічних спостережень свідчить про те, що кромони мають своє місце в комплексі лікування БА, але при легкому перебігу або при відході від ІГКС («сходинка вниз»).
З метою досягнення належного контролю над БА у дітей з тяжкою персистуючою формою можливе використання нового покоління препаратів — гуманізованих моноклональних антитіл до IgE; які рекомендовані для тривалої терапії та спроможні зменшити частоту тяжких загострень.
Персистуючий середньотяжкий і тяжкий перебіг БА характеризується частими нападами, в тому числі нічними, а тому якість життя дитини — незадовільна. З метою запобігання нападам та контролю над станом бронхів хворим із персистуючим перебігом призначають β2-агоністи пролонгованої дії (сальметерол) в режимі кожні 12 годин та надають переваги готовим комбінованим формам (з ІГКС); оскільки препарати сальметеролу застосовуються лише за умови, що дитина отримує базисну терапію ІГКС; а також у пацієнтів старших 4 років.
В окремих випадках для досягнення контролю над астмою вдаються до призначення метилксантинів пролонгованої дії; проте ці препарати попри системну дію мають достатньо широкий спектр побічних ефектів, що суттєво звужує зону їх використання.
Таким чином, складання плану лікування конкретному маленькому пацієнту із БА (базисна, тривала бронходилятаційна терапія, купування загострення) має на меті досягнути контролю над хворобою, що означає покращення якості життя пацієнта. Лікар у динаміці відстежує ефективність стартової терапії та визначає рівень контролю.
Критерії оцінки рівня контролю БА передбачають:
- контрольована: денні симптоми відсутні або з частотою ≤2 епізодів на тиждень, нічні симптоми відсутні, відсутня потреба в препаратах невідкладної допомоги або ≤2 епізодів на тиждень, показники функції дихання (ПОШв або ОФВ) в нормі;
- частково контрольована: денні симптоми з частотою >2 епізодів на тиждень, є нічні симптоми, є потреба в препаратах невідкладної допомоги >2 епізодів на тиждень, показники функції дихання (ПОШв або ОФВ) <80% від норми, 1 або більше загострень в рік;
- неконтрольована: наявність 3 і більше ознак частково контрольованої БА, будь-який тиждень із загостренням.
Для лікаря важливо визначити ступінь контролю над астмою, щоб узгодити терапію. При цьому користуються рекомендаціями GINA, що передбачають збільшення або зменшення обсягу лікування (см. табл).
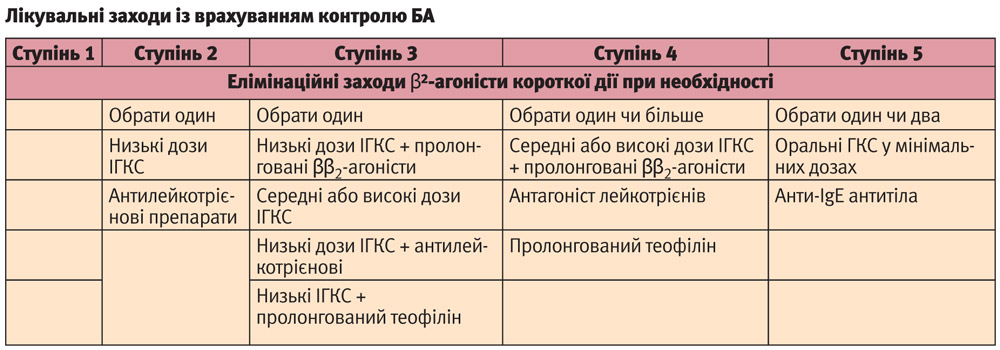
При виборі базисної терапії переважно розпочинають із другого або третього ступеня впродовж 6 тижнів, за умови адекватної відповіді на початкову терапію її продовжують у тому ж дозуванні впродовж 3 місяців.
У ході лікування БА лікар дотримується двох принципів: «сходинка вгору» — обсяг, дозування медикаментозної терапії переглядається, піднімаючись на одну сходинку в лікуванні вверх за умови відсутності повного контролю. У випадку досягнення контролю в лікуванні БА протягом 3 місяців — «сходинка вниз», що означає перегляд обсягу терапії за складом та дозуванням. Однак базисне лікування має тривати 6 місяців, оскільки раніше не відбувається регресії характерних змін з боку бронхів. Тут виявляється ще одна невирішена проблема: не всі пацієнти, а вірніше сказати — їх батьки, витримують таку тривалість лікування. І з цим слід боротись, насамперед — в доступній формі інформувати батьків про мотивацію і значення тривалості та обсягу терапії БА. За цих обставин особливо зростає необхідність формування партнерських відносин в ланцюгу «пацієнт — лікар — сім’я»; освітні заходи, психологічна підтримка дозволять проводити адекватну терапію БА і за складом, і за тривалістю.
Для оцінки досягнення контролю над перебігом БА, окрім клінічних критеріїв, рекомендують застосовувати опитувальник АСТ-тест (Asthma Control Test), який містить 4 запитання, на які відповідає дитина, та 3 — для батьків. Відповіді оцінюють в балах та підсумовуються: якщо пацієнт набирає 20 і більше балів — БА вважається контрольованою, якщо 19 і менше балів — БА недостатньо контрольована. Опитування з використанням АСТ-тесту зручне в ході лікування як допоміжний критерій його ефективності та сприяє доброму становленню партнерських відносин.
Ефективність лікування БА у дітей значною мірою залежна від правильної техніки інгалювання препаратів. На сучасному етапі завдяки співпраці педіатрів та алергологів подоланий страх перед інгаляторами і хворі діти в переважній більшості отримують топічну (інгаляційну) терапію, що є суттєвим поступом в терапії. Однак залишається висока частота неефективної інгаляційної терапії, оскільки не використовуються пристрої для доставки медикаментів до місця ураження. Мова йде про використання спейсерів та небулайзерів при веденні БА. Хворим віком до 4 років рекомендовано користуватись дозованими аерозольними інгаляторами із спейсером з маскою для обличчя (альтернативним пристроєм є — небулайзер із маскою); дітям у віці 4–6 років — дозованим аерозольним інгалятором зі спейсером з мундштуком (або небулайзером з мундштуком), старшим 6 років — дозованим сухопорошковим або аерозольним інгалятором, який активується диханням зі спейсером з мундштуком (небулайзер з мундштуком). Поєднання адекватного медикаментозного лікування з правильною технікою інгаляції суттєво підвищує ефективність топічної терапії та зменшує побічні прояви.
Небулайзерна терапія має суттєві переваги у педіатрії: не потребує координації вдиху та видиху; респірабельна фракція >50% (у дозованих інгаляторів — 30–40%); фракція, що затримується у роті та глотці, незначна (в дозованих аерозольних інгаляторах — до 90%); не містять фреону і пропелентів; легкість виконання; зручність; ліки подаються безперервно; відновлення прохідності дихальних шляхів досягається без парентеральних маніпуляцій; сприяє становленню взаєморозуміння з пацієнтом та його батьками; не спостерігаються системні побічні ефекти. Використовуються компресорні небулайзери, що вимагає застосування медикаментів, які випускаються у формі небул або розчину для інгаляцій.
Узагальнивши підходи до ведення БА, приходимо до викладення практично ступеневого підходу, коли у відповідності до конкретної тяжкості хвороби складається обсяг лікувальних заходів. Однак є випадки, коли цей принцип не спрацьовує, і тому запроваджені критерії досягнення контролю свідчать про його відсутність. Водночас невирішеною залишається проблема індивідуального підходу до вибору обсягу і складу терапії. Кожний пацієнт вирізняється не лише особливостями внутрішніх органів, конституційним характеристиками, даними генетичного анамнезу тощо. В практичній діяльності лікар-педіатр чи алерголог має пам’ятати та проводити корекцію лікувальних заходів із врахуванням:
- віку пацієнта,
- функціональної активності імунної системи,
- структури супутньої патології,
- психологічного портрету дитини,
- рівня контролю астми.
Вікові аспекти визначають клінічні особливості перебігу безпосередньо БА, наприклад загострення у дітей раннього віку частіше перебігає за типом підгострої бронхообструкції, а у дошкільнят та школярів — за гострим типом. Окрім того, є вікові обмеження до застосування окремих медикаментів (β2-агоністи пролонгованої дії не використовуються у пацієнтів молодших 4 років тощо), вибору техніки інгалювання (бебіхалер, спейсер чи небулайзер з маскою або мундштуком), що зрештою і визначає склад та дозування терапії (насамперед ІГКС).
Урахування психологічного портрету дитини — надзвичайно важливе в клінічній практиці
Неможливо не врахувати структуру супутньої патології, яка може бути не лише алергічного ґенезу. Будь-яке поєднання БА та іншої соматичної патології зумовлює перегляд та корекцію протокольної терапії. Наприклад, за результатами власних досліджень, при тяжких формах ядухи часто діагностують вторинний остеопороз або остеопенію, тому такі хворі мають показання до призначення препаратів кальцію (з вітаміном Д), корекції дози та тривалості ІГКС, дозованого фізичного навантаження, вилучення препаратів та продуктів харчування, що мають здатність викликати кальційпенічні стани. В кожному конкретному випадку беруться індивідуальні варіанти корекції, але при цьому має бути витриманий в основному протокол ведення БА та адекватний, однак ощадний — супутньої патології.
Особливого коментаря потребує кваліфікований підхід до оцінки функціональної спроможності імунної системи у кожного пацієнта в залежності від віку. Ні для кого не є новиною, наскільки часто деякі лікарі та переважна більшість батьків прагнуть «стимулювати або підтримати імунітет» у дитини, яка страждає БА. В цьому вбачається надто велика небезпека, насамперед тому, що процеси імуногенезу в дитячому віці характеризуються динамічністю та нарощенням темпів специфічної відповіді. Водночас вони мають певні критичні періоди становлення, що є важливим для формування імунологічної резистентності людини. Саме з цих міркувань втручатись у механізми системної імунної відповіді (на тлі атопічної патології — БА) неприпустимо. І лише в тих випадках, коли є чіткі клініко-лабораторні показання, може проводитись диференційована імуномодуляція. З іншого боку, функціональна активність імунної системи визначає показання та ефективність здійснення алергенспецифічної імунотерапії. Становлення імунної системи здебільшого завершується до 6-річного віку дитини, а тому алергенспецифічна імунотерапія проводиться після 5 років. Однак є частка дітей, в яких функціональне становлення імунної системи завершується у віці до 9–10 років, «пізно стартуючі» в цьому аспекті пацієнти. Саме в них проведення специфічної імунотерапії, розпочате в 5 років, буде неефективним, оскільки імунна система ще не спроможна формувати толерантність.
Урахування психологічного портрету дитини — надзвичайно важливе в клінічній практиці. Воно допомагає виявити характерологічні особливості кожної окремої дитини, сформувати правильну її та батьків реакцію на хворобу, що в сукупності сприяє підвищенню якості життя дитини. На сучасному етапі БА достатньо добре піддається лікуванню, і в більшості хворих вдається досягнути контролю над її перебігом, а тому наше завдання (в тому числі) — допомогти подолати страх батьків перед цим діагнозом, навчити дитину жити з цією патологією, і тільки тоді ми зможемо спільними зусиллями подолати хворобу.
Література
- Антипкін Ю. Г., Надточій Т. Г. Сучасні погляди на етіопатогенез, клініко-діагностичні та лікувально-профілактичні особливості перебігу запального процесу при неспецифічних захворюваннях органів дихання у дітей // Перинатология и педиатрия. – 2011. – № 1(45). – С. 18-23.
- Аллергология и иммунология / Под ред. А. А. Баранова и Р. М. Хаитова: Союз педиатров России. –2-е изд., испр. и доп.– М.: Союз педиатров России, 2010. – 248 с.
- Банадига Н. В., Рогальський І. О. Порушення процесів мінералізації кісткової тканини у дітей на тлі бронхіальної астми // Перинатология и педиатрия. – 2010.– № 3 (43).– С. 89-91.
- Клінічні настанови з діагностики та лікування бронхіальної астми у дітей // Здоров’я України.–2010, №3 (жовтень).– С.38-42.
- Global strategy for asthma management and prevention /National institutes of health. National Heart, lung and Blood institute // Revised. – 2011. – 124 p.


коментарів