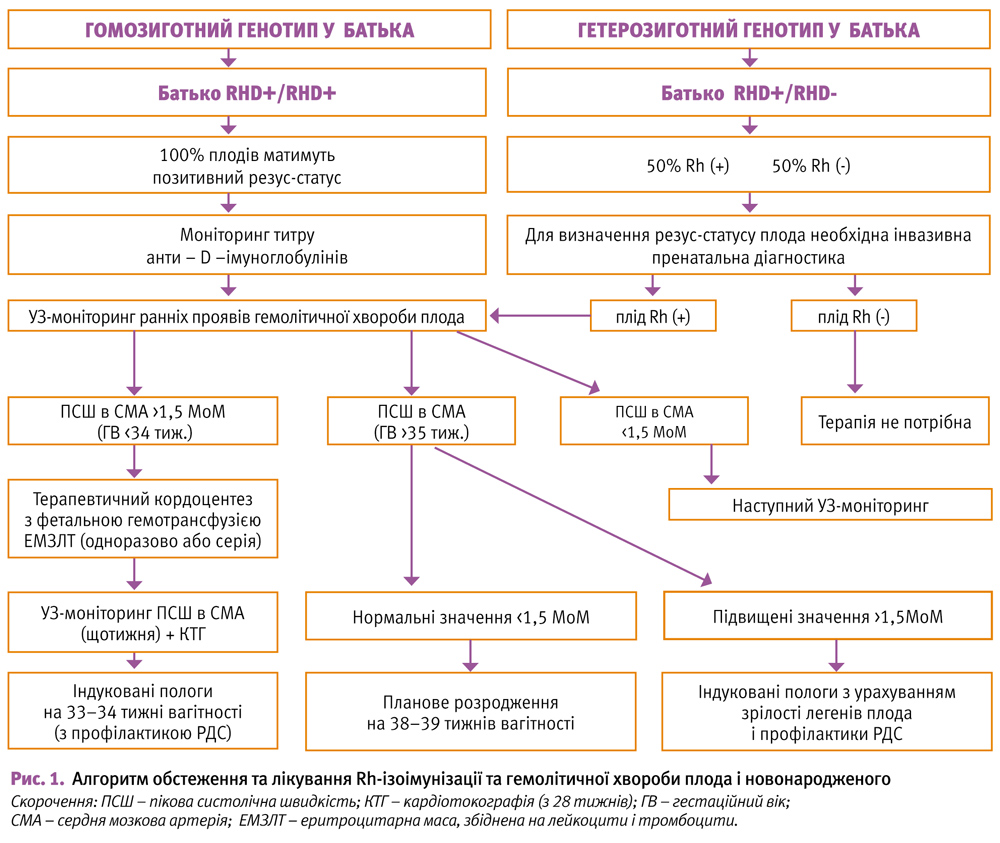
 RH-ізоімунізація – гуморальна імунна відповідь на еритроцитарні антигени плода Rh-групи, включаючи Сс, Dd і Ее (кодуються Rh-алелями), з проникненням антитіл, що утворюються,через плаценту, що викликає екстраваскулярний гемоліз (опсонізація еритроцитів плода антитілами жінки і фагоцитоз еритроцитів) і анемію, а також призводить до екстрабластозу плода, зростання білірубіну й характерної клінічної картини гемолітичної хвороби з токсичним ураженням життєво важливих органів – мозку, печінки, нирок, селезінки продуктами гемолізу.
RH-ізоімунізація – гуморальна імунна відповідь на еритроцитарні антигени плода Rh-групи, включаючи Сс, Dd і Ее (кодуються Rh-алелями), з проникненням антитіл, що утворюються,через плаценту, що викликає екстраваскулярний гемоліз (опсонізація еритроцитів плода антитілами жінки і фагоцитоз еритроцитів) і анемію, а також призводить до екстрабластозу плода, зростання білірубіну й характерної клінічної картини гемолітичної хвороби з токсичним ураженням життєво важливих органів – мозку, печінки, нирок, селезінки продуктами гемолізу.
У МКБ-10 цей стан зареєстровано під кодом Р55 «Гемолітична хвороба плода та новонароджених» та Р 55.0 «Резус-ізоімунізація плода та новонароджених». Частота виникнення гемолітичної хвороби (ГХ) становить 1,5% від усіх вагітностей, частота у пологах – 1:200–300.
Діагностика гемолітичної хвороби плода
Окрім врахування анамнезу, оцінка та діагностика резус-імунізації вагітної традиційно базується на визначені титру антитіл RH-негативної жінки, чоловік якої RH-позитивний. Критичною межею, після якої можливий розвиток клінічно значимої форми ГХ плода, є титр 1:32. Негативними прогностичними ознаками є наростання титру антитіл, «стрибаючий» титр антитіл та їх поява у І триместрі вагітності. Величина титру резус-антитіл не завжди відображає ступінь тяжкості резус-конфлікту та вірогідність виживання плодів/новонароджених з ГХ. При численних вагітностях показник титру антитіл не має кореляції зі ступенем тяжкості ГХ. Крім того, існує декілька станів, при яких титр антитіл втрачає свою інформативність.
Велике значення у діагностиці ГХ плода має ультразвукове дослідження (УЗД), що дозволяє виявити зміни як у товщині плаценти, так і в стані плода. Кожному терміну гестації відповідає певна товщина плаценти, розміри окружності живота та печінки плода.
УЗД у вагітних з резус-сенсибілізацією необхідно проводити, починаючи з 18–20 тижнів. До цього терміну ультразвукові ознаки ГХ плода, як правило, не визначаються. До 32 тижнів повторні УЗД проводяться через кожні 2–4 тижні, у подальшому – кожні 1–2 тижні. При підозрі на тяжку форму ГХ плода інтервал між дослідженнями може скорочуватися до 1–3 днів. У кожної вагітної терміни повторних сканувань визначаються індивідуально.
Анемія плода не має патогномонічних ехографічних ознак, і навіть важкі ступені її вираженості можуть не супроводжуватися розвитком водянки. При ГХ плода по мірі зростання тяжкості захворювання спостерігається збільшення товщини плаценти. Перевищення нормальної для терміну вагітності товщини плаценти на 0,5–1,0 см є однією з ранніх ознак ГХ плода. Характерними для ГХ плода ультразвуковими критеріями також є збільшення розмірів печінки і селезінки плода.
Найбільш точно при УЗД діагностується набрякова форма ГХ плода, критеріями якої є:
- виражена плацентомегалія;
- гепатоспленомегалія;
- асцит;
- багатоводдя.
При вираженій водянці плода спостерігаються, крім цього, кардіомегалія і перикардіальний випіт, гідроторакс, підвищена ехогенність кишківника внаслідок набряку його стінки, набряк підшкірної клітковини голови («подвійний контур» голівки), тулуба і кінцівок плода.
Додатковим ультразвуковим критерієм тяжкості захворювання плода може служити розширення вени пуповини (більше 10 мм).
У діагностиці важкої анемії плода є ще один важливий момент – трикуспідальна регургітація, яка передує асциту і набряку плода. Використання цієї патологічної ознаки може допомогти у зниженні кількості хибнопозитивних результатів. Якщо у плода, що має ризик розвитку анемії, з нормальними значеннями пікової систолічної швидкості (ПСШ) кровотоку в середньомозковій артерії (СМА), визначається трикуспідальна регургітація – найвірогідніше, у нього анемія.
Практично всі УЗ-маркери, крім показника ПСШ у СМА, виміряного за допомогою доплерометрії, мають низьку чутливість, пізню маніфестацію і різну специфічність, та не можуть використовуватися в якості раннього предиктора, який прогнозує розвиток ГХ плода. У деяких ситуаціях УЗ-метод єдино можливий для спостереження за станом плода. Зокрема, при підтіканні навколоплідних вод, відсутності технічних можливостей для проведення амніоцентезу і кордоцентезу, при забрудненні навколоплідних вод кров’ю або меконієм, при відмові пацієнтки від інвазивних процедур.
Функціональний стан плода у вагітних із резус-сенсибілізацією оцінюють, використовуючи також кардіотокографію і біофізичний профіль плода, які доцільно проводити в амбулаторних умовах, починаючи з 30–32 тижнів вагітності і до розродження. За наявності ознак порушення стану плода моніторинг необхідно проводити щодня з метою визначення подальшої тактики ведення та часу розродження.
При КТГ відзначаються характерні для гіпоксії плода зміни, ступінь вираженості яких збільшується по мірі наростання важкості гемолітичної хвороби плода. Реєстрація при КТГ кривої «синусоїдального» типу свідчить про наявність тяжкої форми гемолітичної хвороби і вкрай важкого стану плода. Однак КТГ у ізольованому використанні не має суттєвого діагностичного значення, оскільки ознаки тяжкості стану плода на кривих КТГ з’являються значно пізніше, ніж при доплерометрії у СМА.
Оцінка ступеня тяжкості ГХ плода ґрунтується у тому числі і на інвазивних пренатальних втручаннях (амніоцентез, кордоцентез). Амніоцентез при ГХ плода проводиться вже з 22–24 тижнів вагітності під УЗ-контролем для запобігання травматизації плаценти або пуповини. При травмі виникає кровотеча у плода і матері, що збільшує ступінь імунізації. Отриману амніотичну рідину піддають спектрофотометричному аналізу (після виконання амніоцентезу вагітній необхідно ввести антирезусний Д-глобулін у дозі 300 мкг).
Діагностична цінність амніоцентезу обумовлена тим, що при ГХ за рахунок гемолізу еритроцитів відбувається підвищення концентрації білірубіну в крові плода (у сечі, в навколоплідних водах) і, відповідно, оптичної щільності білірубіну (ОЩБ) в амніотичній рідині. ОЩБ в амніотичній рідині визначають з 24 тижнів вагітності за допомогою спектрофотометра з довжиною хвилі від 400 до 700 нм і отримані дані аналізують відповідно до модифікованої шкали Лілі, яка передбачає додатковий розподіл зони 2 шкали Лілі на три сегменти – A, B і C, що дозволяє уточнити показання до кордоцентезу (при відповідності значень ОЩБ зонам 2B і 2C), і тим самим підвищити діагностичну значимість методу.
Якщо значення ОЩБ відповідає 1-й зоні, то у плода можна виключити ГХ. Чим ближче величина ОЩБ до 3-ї зони (2C), тим ймовірніша важка ступінь захворювання плода, і навпаки, чим далі розташована величина ОЩБ від 3-ї зони (2A), тим менш імовірна ГХП. У залежності від величини ОЩБ по відношенню до відповідних зон шкали, рекомендуються подальші діагностичні заходи: якщо значення ОЩБ знаходяться в зоні 2A, то амніоцентез необхідно повторити через 4 тижні; при відповідності зоні 2B процедуру проводять через 1–2 тижні; значення ОЩБ, що знаходяться у межах зони 2C і 3-ї зони, є показанням до діагностичного кордоцентезу і, можливо, внутрішньоутробного переливання крові.
У даний час амніоцентез становить історичний інтерес і має відносну цінність, оскільки він неінформативний при апластичній анемії у плода. Його використовують тільки у якості додаткового методу при виконанні діагностичного кордоцентезу.
Оптимальним діагностичним тестом ГХ плода є дослідження крові плода, отриманої шляхом кордоцентезу. Аналіз 1–2 мл крові плода дає можливість визначити резус належність, гематокрит (Ht), гемоглобін (Нb), кількість еритроцитів, білірубін, кислотно-лужну рівновагу (КЛР), кількість ретикулоцитів, рівень сироваткового білка, а також антитіла, пов’язані з фетальними еритроцитами.
Зниження гематокриту на 15% від норми свідчить про тяжкість захворювання і служить однією з визначальних ознак у показаннях до внутрішньоутробного переливання крові (ВПК). Показники кислотно-лужної рівноваги дозволяють виявити гіпоксію плода.
Визначення кардіотропоніну Т у крові плода з ГХ дозволяє зробити прогностичну оцінку стану його серцево-судинної системи, при позитивному тесті прогноз несприятливий. у таких випадках ВПК малоефективні. Кордоцентез здійснюється під контролем УЗД, і за відповідного досвіду не передбачає великих труднощів.
Показаннями до кордоцентезу, який при ізоімунізаціі і анемії плода зазвичай проводиться з 24 тижнів вагітності (але можливо і раніше – з 20 тижнів), є відповідність рівня ОЩБ зоні 3 або 2С шкали Лілі, ультразвукові маркери ГХ плода, підвищення максимальної систолічної швидкості кровотоку в СМА плода, рідше обтяжений акушерський анамнез (анте-, інтра-, постнатальна загибель дітей від ГХ або факт кількаразових замінних переливань крові у неонатальному періоді), титр антитіл більший від 1:16.
До 2000 року стандартом ведення плода з ризиком анемії була інвазивна тактика відповідно до акушерського анамнезу або по досягненні «критичного титру AТ».
Останнім часом стало можливо більш точно передбачити анемію плода з використанням неінвазивної методики: вимірювання пікової систолічної швидкості (ПСШ) у середній мозковій артерії (СМА). Дослідження G. Mari (1987 р.) показали високу ступінь кореляції між гематокритом і максимальною швидкістю кровотоку в середньомозковій артерії. Діагностичне значення даного методу визначається тим, що в результаті анемії і, відповідно, гіпоксії у плода виникає периферична вазодилятація і стимуляція хеморецепторів. Це призводить до збільшення скорочувальної здатності міокарда і, отже, збільшення серцевого викиду.
Поряд з цим при ГХ плода відбувається зниження в'язкості крові, що, у свою чергу, сприяє збільшенню венозного повернення і серцевого викиду. Таким чином, виникає гіпердинамічний стан кровообігу і максимальна швидкість кровотоку в середній мозковій артерії плода збільшується, корелюючи з тяжкістю анемії у плода при ГХ.
Метод допплерометрії ПСШ у СМА плода високо відтворений, найбільш точний, достовірний з низьким хибнопозитивним результатом, однак, вимагає суворого дотримання методики вимірювання. Цей критерій, оцінений у динаміці, в даний час використовується як маркер тяжкості анемії у плода для визначення оптимальних термінів початку інфузій та їх повторів при анемічній формі гемолітичної хвороби. Оптимальне граничне значення пікової систолічної швидкості кровотоку, що характеризує легку анемію – 1,2–1,4 Мом, анемію середньої тяжкості – 1,4–1,50 Мом, важку анемію – >1,55 Мом. Пікова систолічна швидкість кровотоку 1,5 Мом і більше відповідає анемії середнього або важкого ступеня з чутливістю 100% і частотою хибнопозитивних результатів 12%. Більш простим способом для швидкого визначення порогового значення ПСШ (см/сек) в СМА, відповідного 1,5 МоM, є подвоєння терміну вагітності (тижнів), при якому проводиться УЗД. Отримана величина практично буде відповідати 1,5 Мом – ПСШ в СМА, виміряної в см/сек. Однак, для найбільш точного розрахунку краще використовувати спеціальні таблиці або електронний калькулятор (www.perinatology.com/ calculators/MCA.htm). У разі відповідності максимальної швидкості кровотоку в СМА рівню медіани значень для терміну вагітності, повторні вимірювання проводять через 2 тижні, при збільшенні швидкості до 1,2 Мом – через 7–10 днів, при швидкості 1,2–1,4 Мом – через 5–7 днів. Якщо швидкість становила 1,5 Мом, виконується кордоцентез з метою діагностики анемії у плода та підбору донора.
Розрахунок гемоглобіну плода в МОМ здійснюється за формулою на основі показника ПШ в СМА: Y = 1,185–0,341x, де Y – гемоглобін плода (МОМ), Х – максимальна швидкість кровотоку в середній мозковій артерії у плода (МОМ). Отриманий результат розцінюється таким чином: Hb <0,84 МоM – легкий ступінь анемії; <0,65 МоM – середня і <0,55 МоM – важка.
Вимірювання максимальної швидкості кровотоку в СМА та застосування цього критерію для діагностики анемії плода є одним з відкриттів фетальної медицини, яке значно змінило стандарти курації вагітних з ізоіммунізацією та ГХ плода. Це дозволило більш ніж на 70% знизити кількість інвазивних процедур, частина з яких супроводжуються втратою вагітності, і значно поліпшити перинатальні наслідки при іммуноконфліктній вагітності.
Продовження
у наступному номері.


коментариев