Выбор, основанный на доказательствах
Медикаментозный аборт (МА) с применением мифепристона и простагландина был впервые одобрен для практического применения в 1988 году и теперь используется более чем в 40 странах [1]. Учитывая особую значимость препаратов для прерывания нежелательной беременности в связи с их высокой востребованностью, эффективностью и безопасностью, ВОЗ включила мифепристон (2005 г.) и мизопростол (2009 г.) в перечень основных лекарственных средств (14th и 16th Model List of Essential Medicines) [2].
Многолетний опыт клинического применения и научных исследований способствовали накоплению новых знаний о технологии метода и пересмотру ряда позиций в отношении режимов применения препаратов, сроков беременности для прерывания, наблюдения и ведения восстановительного периода, что было реализовано в оптимизации его протокола. Обновленные клинические протоколы медикаментозного прерывания нежелательной беременности были разработаны в 2011–2012 гг. и рекомендованы такими авторитетными организациями как Королевское и Американское общества акушеров-гинекологов, а также ВОЗ.
Учитывая высокий интерес специалистов к этому вопросу, предлагаем вашему вниманию дайджест наиболее значимых зарубежных публикаций, составивших доказательную базу для такого пересмотра.
Первые клинические исследования по выбору дозировки мифепристона проводились с использованием доз от 200 до 800 мг. Была продемонстрирована эффективность в диапазоне 63–87% (без использования простагландина). Никакого увеличения эффективности не наблюдалось при дозах выше 600 мг или при введении повторных доз [3–5].
Использование низких доз мифепристона (повторно по 50 мг, суммарная доза – 150 мг) также продемонстрировало достаточную эффективность и широко используется в Китае. Однако были показаны некоторые клинические преимущества одной дозы (несколько выше эффективность) [6–7].
Мифепристон без использования мизопростола оказался менее эффективен по сравнению с комбинацией мифепристон/простагландин (ОР 3,76 при 95% ДИ 2,30 до 6,15) [14]. Поэтому для достижения приемлемого клинического результата была предложена комбинированная схема.
Таким образом, была зарегистрирована разовая доза 600 мг мифепристона в комбинации с простагландином (ПГ) в утвержденных режимах МА во всех странах, где мифепристон был тогда разрешен, за исключением Китая.
Однако в обзоре C. Fiala (2006) [8] отмечается, что «первоначальной основной задачей, при введении МА в клиническую практику, было найти определенный эффективный режим, а это значит, что дозы мифепристона и ПГ, возможно, были выше, чем необходимо». Поэтому дальнейшие исследования были сосредоточены на двух аспектах: сокращение дозы мифепристона и побочных эффектов метода. Мета-анализ, проведенный в 2009 г. Lievre M. с соавт. [9] на основании анализа 4-х РКИ (3482 пациентки) при беременности в сроках до 63 дней, подвел итог 15-летним исследованиям и не показал достоверной разницы в увеличении частоты неудач при сравнении доз 200 и 600 мг (разница 0,4%, 95% ДИ = -0,3% до 1,0%). Недостоверное увеличение частоты продолжающейся беременности (но не более 1%) в этих исследованиях было обусловлено разницей в сроках беременности (до 63 дней), а не дозой мифепристона. Отмечено, что замена орального пути введения мизопростола на сублингвальный, буккальный или вагинальный приводит к уравниванию результатов эффективности в этих сроках.
На основании нескольких РКИ и мета-анализов, опубликованных в Базе Кокрейна (последний – в 2011 г.), было продемонстрировано, что эффективность метода составляет 96–98% независимо от введенной дозы мифепристона (ОР 1,07, 95% ДИ 0,87–1,32) [10], что послужило основанием для пересмотра рекомендаций по выбору минимально необходимой эффективной дозы мифепристона, которая определена в 200 мг. В настоящее время именно этот режим рекомендуется и широко используется в клинической практике во всех странах Европы и США [11, 12], а сравнительные исследования эффективности доз 200 и 600 мг больше не проводятся ввиду несомненности полученных доказательств.
В отличие от мифепристона, дозы и пути введения мизопростола не являются константой и зависят от срока прерываемой беременности. В период регистрации метода МА и используемых препаратов для его осуществления максимальный срок для прерывания беременности этим методом был 7 недель (до 49 дней аменореи), при этом использовалось 400 мкг мизопростола, вводимого внутрь. Попытки прерывания беременности в больших сроках с использованием указанного режима привели к констатации снижения эффективности метода. Так, по данным EMEA (2007), некоторое снижение эффективности методики наблюдается в сроках 50–63 дня при приеме мизопростола внутрь. Это обусловлено особенностями фармакокинетики препарата: достижение пиковой концентрации — 12 минут, период полувыведения — 20–40 минут, а, следовательно, оказывается коротким его клиническое действие. Этот факт стимулировал исследования по пролонгированию сроков его действия. Было показано, что сублингвальный прием увеличивает пиковую концентрацию действующего вещества в крови, а вагинальный – способствует более медленному ее снижению, поэтому оба пути введения способствуют увеличению эффективности. Так, доказано, что прием мизопростола внутрь менее эффективен, чем вагинальный (ОР 3,00, 95% ДИ 1,44 до 6,24), а сублингвальное и буккальное введение были одинаково эффективны по сравнению с вагинальным путем [14]. В то же время обнаружено, что пероральный прием мизопростола чаще ассоциировался с тошнотой и диареей, чем внутривлагалищное введение (2 исследования, ОР 1,13, 95% ДИ 1,0–1,25; ОР 1,80, 95% ДИ 1,49–2,18 соответственно) [14]. Введение повторных доз через 3 часа для повышения эффективности метода оказалось успешным в поздние сроки беременности (эффективность от 95,4% до 98,5% и снижение числа продолжающейся беременности с 1,5% до 0,1% по сравнению со стандартной разовой дозой мизопростола) [15], но не показало преимуществ в первом триместре.
Изучение различных типов простагландинов, доз, кратности и путей введения мизопростола в исследованиях на протяжении 20 лет привели к разработке новых схем МА в зависимости от сроков беременности, которые отражены в клинических рекомендациях RCOG (2011), ACOG (2011) и ВОЗ (2012) [11, 12, 1]. Таким образом, в настоящее время для прерывания медикаментозным методом доступны все сроки беременности, разрешенные законом в тех странах, где зарегистрированы мифепристон и мизопростол (табл. 1), а рекомендованной единственной дозой мифепристона во всех сроках (до 22 недель) является 200 мг. В зависимости от срока прерывания беременности меняется кратность применяемой дозы мизопростола.
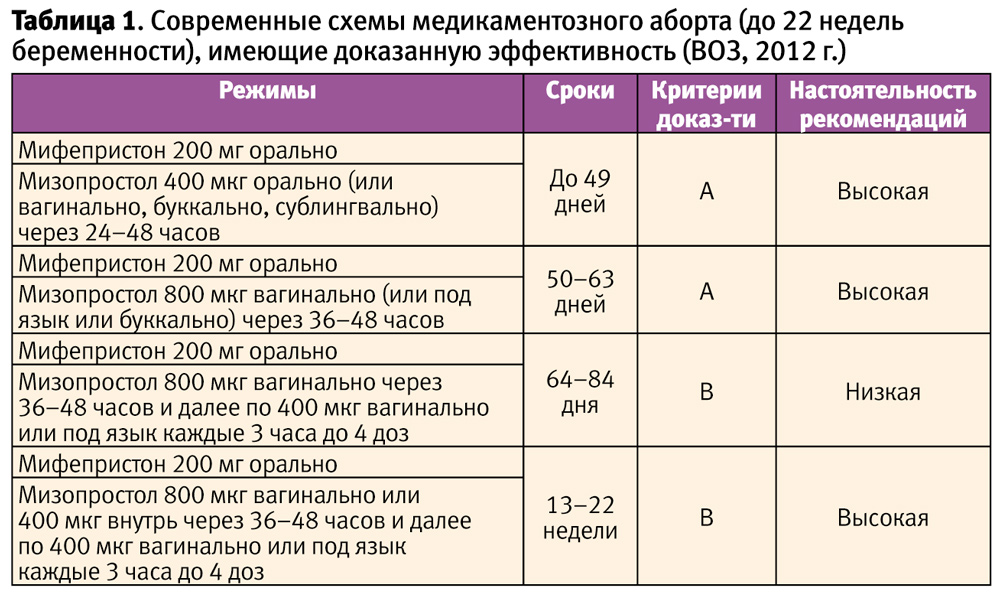
Эффективность медикаментозного аборта с использованием рекомендованных схем, достигает, по данным разных авторов, до 98,9%, что отражено в Руководстве ВОЗ 2012 г. [1]. При анализе источников литературы, опубликованных ранее, следует учитывать, что разница в приводимых в них сведениях об эффективности метода находится в зависимости от использованных режимов (в том числе других, кроме мизопростола, простагландинов) и сроков прерываемой беременности.
Медикаментозный аборт с применением мифепристона и мизопростола отличается высоким уровнем безопасности. Комплексное изучение токсикологии, которое было проведено еще до утверждения мифепристона, не выявило истинную токсичность при лечении у крыс и обезьян в течение одного и шести месяцев [17]. Безопасность для одноразового использования у людей была подтверждена в большом исследовании в 16173 случаев медикаментозного аборта [4]. Безопасность долгосрочного использования была установлена в ряде исследований для других показаний, включая миому матки, эндометриоз, рак молочной железы и менингиому [18–22].
Уровень материнской смертности является основным критерием оценки безопасности аборта. В целом FDA зарегистрировано 14 случаев материнской смерти после выполнения медикаментозного аборта на фоне 1,52 млн. (2011 г.) [23] абортов, выполненных в США этим методом, что составляет 0,009% (или 0,9 на 100000 вмешательств). Частота осложнений после медикаментозного аборта в среднем составляет 5% (0,2–7,2%), из них примерно в 3% случаев требуется вакуумная аспирация.
Медикаментозный аборт не связан с травматическим повреждением матки, ее шейки и эндометрия, риском анестезиологического пособия, а также инфекционными осложнениями (0,5%).
В отличие от дилатации и кюретажа, при МА не было найдено доказательств увеличения риска внематочной беременности (1,04; 95% ДИ 0,76 до 1,41), спонтанного аборта (0,87; 95% ДИ 0,72 до 1,05), преждевременных родов (0,88; 95% ДИ 0.66 до 1,18) или низкого веса при рождении (0,82; 95% ДИ – 0,61 до 1,11) независимо от гестационного срока [24–25].
Достоверных статистических данных о связи аборта с бесплодием, раком молочной железы и раком шейки матки в настоящее время не существует [26]. Исследование, опубликованное в The Lancet (2004), в рамках совместного повторного анализа: мета-анализ 53 эпидемиологических исследований 83000 женщин с раком груди в 16 странах не подтвердил взаимосвязь между абортами и раком груди, с относительным риском (ОР 0,93 95% ДИ 0,89–0,96). По поводу вторичного бесплодия как исхода прерывания беременности, данные указывают, что оно возникает при внебольничных абортах, осложнившихся тяжелыми инфекциями или при наличие ИППП (хламидийная инфекция). Прерывание же беременности в условиях клиники не приводит к утрате фертильности [27].
Инфицирование верхних половых путей во время хирургического аборта, в том числе матки и маточных труб, может вызвать воспалительные осложнения после абортов (3,5–7,5%). Показано, что риск постабортных инфекций половых путей у женщин, получающих антибиотики, был ниже на 59%, в отличие от женщин, которые получали плацебо (19 РКИ). Менее определенные данные существуют в отношении необходимости профилактического назначения антибиотиков после медикаментозного аборта (степень доказательности А и С соответственно). Не доказано, что вагинальное применение мизопростола сопровождается увеличением риска септических осложнений [23].
Доказательные данные о влиянии прерывания беременности на гормональный статус (так называемый «гипоталамический стресс») отсутст вуют, равно как и сведения о необходимости «гормональной реабилитации» (однако это не означает, что нет необходимости в проведении консультирования по выбору метода контрацепции, в том числе и гормонального, и раннего начала ее использования).
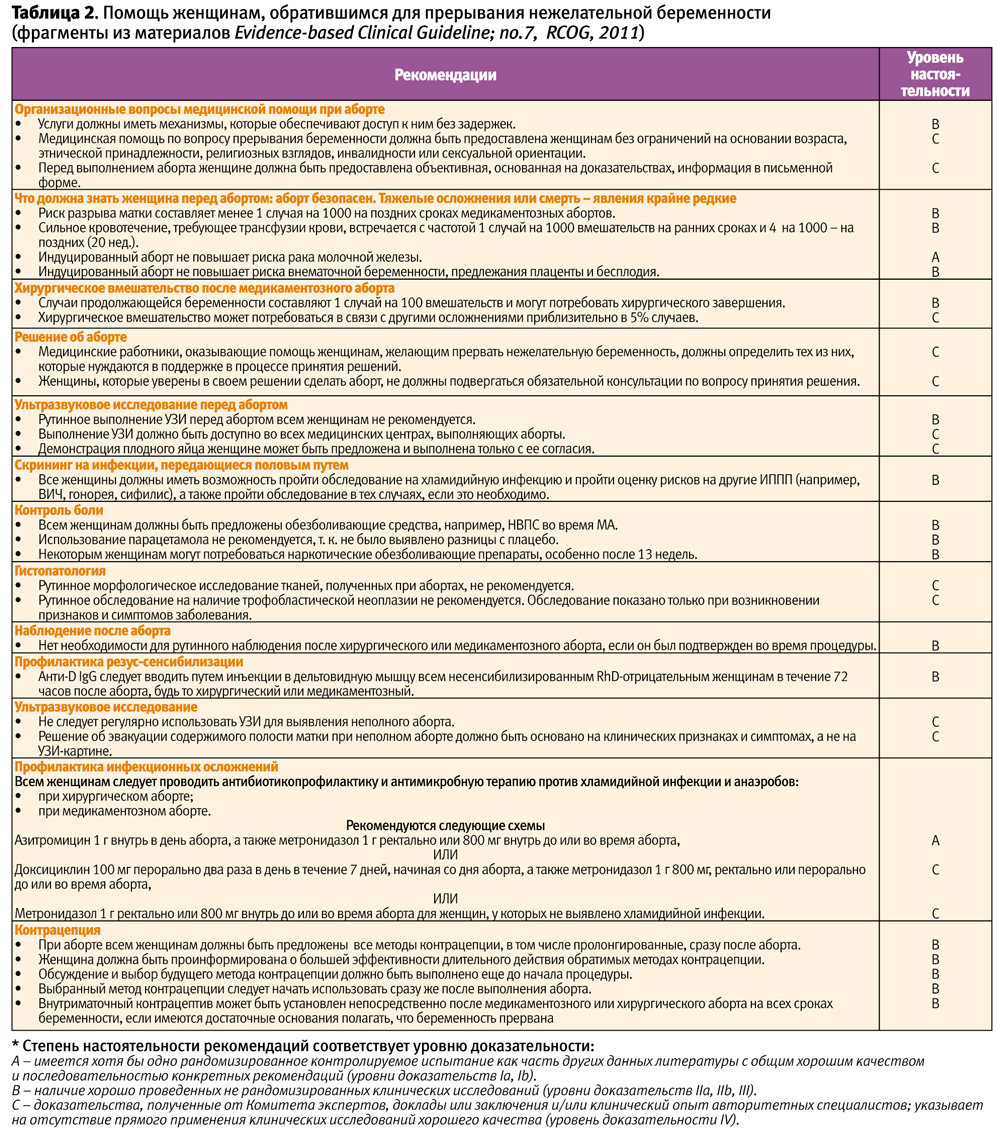
Завершая настоящий обзор, приводим основные положения международных рекомендаций по клиническому ведению МА, которые могут быть применимы для повышения качества медицинской помощи женщинам при нежелательной беременности и ее прерывании медикаментозным или хирургическим (вакуумная аспирация) методами (табл. 2).
Список литературы находится в редакции.
