 Викидень, що не відбувся (вагітність, що завмерла; пусте плідне яйце; анембріонія; рання загибель плода; ембріональна/плодова загибель) – підтверджене за допомогою УЗД припинення розвитку вагітності із затримкою плодових тканин в матці за відсутності кровотечі
Викидень, що не відбувся (вагітність, що завмерла; пусте плідне яйце; анембріонія; рання загибель плода; ембріональна/плодова загибель) – підтверджене за допомогою УЗД припинення розвитку вагітності із затримкою плодових тканин в матці за відсутності кровотечі
Викидень, що не відбувся – це патологічний симптомокомплекс, що включає:
1) нежиттєздатність плода (ембріона) при очікуваному терміні вагітності ³4-х тижнів;
2) патологічну інертність міометрія;
3) порушення у системі гемостазу.
Епідеміологія
Мимовільним перериванням завершуються від 20% до 35% бажаних вагітностей. Приблизно у половини пацієнток зі спонтанним припиненням гестації діагностують викидень, що не відбувся. Таким чином, з числа діагностованих бажаних вагітностей кожна п'ята зупиняється у розвитку («завмирає»). Велика частина випадків невиношування вагітностей (до 80%) припадає на I триместр гестації.
Етіологічні чинники
- Порушення анатомії статевих органів.
- вроджені дефекти матки (повне подвоєння матки, одно- або дворога, сідлоподібна, однорога матка, часткова або повна внутрішньоматкова перетинка);
- надбані дефекти матки (істміко-цервікальна неспроможність, субмукозна міома матки, внутрішньо-маткові сінехії).
- Генетичні та хромосомні аномалії ембріона. Слід розглядати доцільність вичікувальної тактики та відмови від терапії, оскільки більшість випадків спонтанного переривання вагітності відбувається на ранніх термінах, найчастіше причиною тому — так званий «генетичний скид», при якому плід нежиттєздатний. У ситуації генетичної неповноцінності ембріона пролонгування вагітності не має сенсу, про що слід обов’язково попередити батьків.
- кількісні хромосомні аберації можуть бути результатом:
- порушення мейозу на будь-якій стадії поділу гамет – випадки нерозходження парних хромосом у яйцеклітинах та сперматозоїдах, при яких виникає моно- або трисомія;
- порушень при заплідненні – диспермія (запліднення яйцеклітини двома та більше сперматозоїдами) з утворенням поліплоїдного зародка (міхуровий занесок);
- порушень під час перших мітотичних поділів заплідненої яйцеклітини, при першому поділі може виникнути повна тетраплоїдія з подвоєнням хромосом без поділу цитоплазми, а на етапі наступних поділів подібні порушення можуть стати причиною мозаїцизму.
- якісні хромосомні аберації:
- реципрокні транслокації – хромосоми взаємно обмінюються ділянками – 50% хромосомних аномалій при вагітності (поширеність 1:1300–1:700 випадків викидня, що не відбувся);
- робертсонівські транслокації – злиття акроцентричних хромосом з повною або частковою втратою матеріалу коротких плечей;
- зміни жіночих статевих хромосом;
- делеції, інверсії та інші порушення.
- Патологічні стани ендометрію, що характеризуються його неповноцінністю та нездатністю забезпечити процеси ґестації, в тому числі в зв'язку з хронічними захворюваннями матері.
- хронічний аутоімунний ендометрит (клініко-морфологічний синдром, комплекс морфофункціональних змін ендометрію запального генезу, які супроводжуються порушенням нормальної циклічної трансформації та рецептивності ендометрію);
- синдром регенераторно-пластичної недостатності ендометрію (атрофія слизової оболонки матки, «ендометріопатія»). Для цього синдрому характерні зниження секреторної активності епітеліоцитів; зниження експресії рецепторів до естрогенів та прогестерону з втратою або різким зниженням їх чутливості; алло- та аутоімунні реакції; «тонкий ендометрій» (leptometrium, менше 7 мм в лютеїновій фазі, що зареєстровано не менше ніж у двох послідовних циклах).
- Порушення згортання крові – спадкові тромбофілії та антифосфоліпідний синдром (АФС).
- антифосфоліпідний синдром
Клінічні критерії (щонайменше одна відповідність)
- Один та більше епізодів тромбозу, підтвердженого за допомогою візуалізуючих методів, допплерівського дослідження або гістологічно.
- Дострокове завершення вагітності:
- незрозумілий спонтанний аборт до 10 тижнів ґестації – три епізоди та більше, пізніше 10 тижнів – один та більше;
- як мінімум, одні передчасні пологи до 34 тижнів ґестації через важку прееклампсію/еклампсію.
Лабораторні критерії (щонайменше одна відповідність)
- Підвищення концентрації IgG/IgM до антикардіоліпіну (більше 40 МО/мл) або до b2-глікопротеїну I (вище 99-го процентилю) щонайменше 2 рази протягом 12 тижнів.
- Виявлення антикоагулянту червоного вовчака щонайменше 2 рази протягом 12 тижнів.
Підозрювати АФС, відповідно до положень консенсусу, слід уже при наявності хоча б одного з критеріїв, представлених нижче.
- Тромбоз.
- Пізній викидень, передчасні пологи.
- Серцеві шуми або вегетації на клапанах серця в анамнезі.
- Гематологічні порушення в анамнезі, такі як тромбоцитопенія, гемолітична анемія.
- Прееклампсія в анамнезі.
- Нетромботичні неврологічні симптоми – головний біль, мігрень, хорея, судоми, поперечний мієліт, синдром Гієна–Барре.
- Невідомої етіології надниркова недостатність.
- Асептичний некроз кісток при відсутності інших факторів ризику.
- Легенева гіпертензія
- Поліморфізм генів гемостазу
- фактора V Лейдена;
- протромбіну G20210A;
- антитромбіну ІІІ;
- мутації метілентетрагідрофолатредуктази (MTHFR).
- Інші
- Аномальна активність природних кілерів (NK-клітин);
- Наявність алоімунних антитіл, таких як антибатьківські цитотоксичні, антиідіотипічні антитіла, що блокують реакції змішаних лімфоцитів.
- HLA-несумісність партнерів.
Фактори ризику
- старший та пізній репродуктивний вік партнерів (>35 років);
- попередні самовільні викидні;
- синдром полікістозних яєчників;
- некомпенсований цукровий діабет;
- хронічні хвороби нирок;
- системний червоний вовчак та інші системні захворювання сполучної тканини;
- некомпенсовані захворювання щитовидної залози (гіпотиреоз);
- тяжка артеріальна гіпертензія;
- порушення репродуктивного здоров'я статевого партнера;
- гострі інфекції (Listeria, токсоплазмоз, парвовірус В19, герпесвірус, краснуха);
- паління;
- алкогольна залежність;
- кокаїнова залежність;
- споживання великих доз кофеїну;
- низький індекс маси тіла (<20 кг/м2);
- стресові ситуації.
Діагностичні критерії
- зникнення нудоти, блювоти, гіперсалівації.
- зникає нагрубання молочних залоз.
Об’єктивно:
Сонографічне обстеження
- діаметр плідного міхура (ДПМ) >20 мм(середнє арифметичне 3-х діаметрів), без фетального полюса (трансвагінальний доступ (ТВД)) або ДПМ >25 мм, без фетального полюса (трансабдомінальний доступ (ТАД)).
- КТР >7 мм, без пульсації серця плоду при ТВД або КТР >8 мм, без пульсації серця плоду при ТАД.
- коли ДПМ £20 мм, без фетального полюса або якщо КТР £7 мм, без пульсації серця плоду і повторний ТВД, організований принаймні за 7 діб від початкового сканування, не демонструє взагалі ніяких змін в розмірах.
- коли ДПМ £25 мм, без фетального полюса або якщо КТР £8 мм, без пульсації серця плоду і повторний ТАД, організований принаймні за 7 діб від початкового сканування, не демонструє взагалі ніяких змін в розмірах.
- відсутність ембріона через 6 тижнів від початку останньої менструації.
Важливий клінічний аспект: відсутність серцебиття плода – не єдина та не обов'язкова ознака вагітності: при малому терміні вагітності серцебиття плоду ще не спостерігають. В такому випадку при підозрі на викидень, що не відбувся, визначення b-хоріонічного гонадотропіну (b-ХГЛ) може застосовуватися для підтвердження життєздатної маткової вагітності. b-хоріонічний гонадотропін – специфічний гормон, що відображає функціональну активність трофобласта, синтез b-ХГЛ при фізіологічній вагітності починається вже через 1 добу після імплантації.
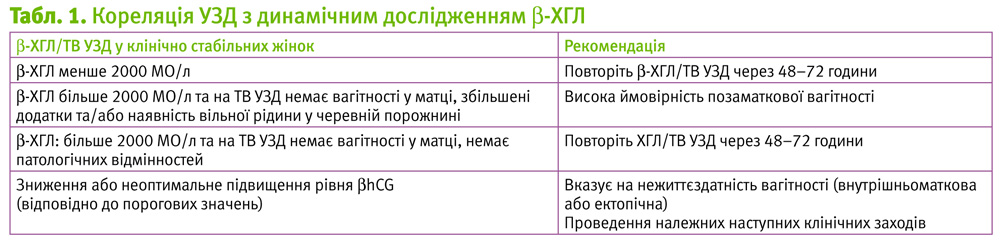
Одноразовий вимір b-ХГЛ незалежно від його значення не дозволяє провести диференціальну діагностику між матковою та позаматковою вагітністю (з життєздатним або нежиттєздатним ембріоном), для вибору лікарської тактики необхідний динамічний контроль цього гормону, щоб уникнути ризику переривання життєздатної маткової вагітності (табл. 1).
У нормі рівень b-ХГЛ при значеннях нижче 1200 мМО/мл подвоюється кожні 2 доби, а при значеннях нижче 6000 мМО/мл – кожні 3 доби. У випадку викидня, що не відбувся, таких змін не відзначається, а b-ХГЛ знижений у 3–9 разів.
Вміст прогестерону при викидні, що не відбувся, може зберігатися на відносно високому рівні.
Додаткове обстеження
Група крові, резус-фактор, загальний аналіз крові (формула крові за потребою), гематокрит, СРБ (при підозрі на наявність інфекції), розширена коагулограма, бактеріологічне дослідження виділень з цервікального каналу у разі потреби.

Лікування
Вичікувальна тактика
Всі медичні працівники повинні бути обізнані про психологічні наслідки, пов'язані з втратою вагітності, та повинні надавати психологічну підтримку, в разі потреби.
Негативний психологічний вплив ранньої втрати вагітності може бути серйозним і тривалим, та зачіпає як жінок, так і їхні сім’ї, може бути різним для кожної сімейної пари.
Вичікувальна тактика часто є початковим вибором лікування для пацієнтів. Проте, жінок, які обирають цей варіант, слід проконсультувати, що повне вигнання може зайняти до 1 місяця.
На 7-у добу після встановлення діагнозу «викидень, що не відбувся», приблизно 50% жінок вимагають хірургічного лікування.
Емоційна стурбованість протягом вичікувального періоду може бути значною. Часто медикаментозне або хірургічне втручання є більш привабливою альтернативою.
Імовірність спонтанного вигнання швидко знижується після 1 тижня вичікування. Тому може бути доцільним запропонувати 1 тиждень очікування, якщо пацієнтка наполягає на тому, з оформленням регламентуючої документації. Термін вагітності також необхідно враховувати (табл. 2).
Медикаментозна терапія
Якщо немає підозр інфекції та розмір матки менше, ніж 12 тижнів:
- мізопростол 800 мкг вагінально (макс. дві дози), другу дозу через 3 години у разі потреби;
або
- мізопростол 600 мкг сублінгвально (макс. дві дози), другу дозу через 3 години у разі потреби.
Або
- хірургічна евакуація вмісту матки шляхом вакуумної аспірації.
Після призначення мізопростолу госпіталізація до стаціонару не є необхідною, оскільки експульсія (вигнання) плода може відбутися або за кілька годин, або за кілька тижнів. Кров’яні виділення можуть бути протягом 2 тижнів.
Скорочення матки звичайно розпочинаються за кілька годин від прийому мізопростолу. Рутиний прийом антибіотиків не рекомендований, проте НПВС або парацетамол можуть бути використані для знеболення (у момент введення мізопростолу та у разі потреби через кожні 6 годин – ібупрофен 800 мг або тайленол 1–2 таб).
Динамічне спостереження за пацієнткою проводять до вигнання плоду. Якщо мізопростол виявився неефективним, від вичікувальної тактики переходять до хірургічної евакуації, про що жінка має бути попереджена попередньо. Якщо немає підозр на інфекцію та розмір матки становить 13 тижнів або більше, можлива медикаментозна або хірургічна евакуація вмісту порожнини матки:
- мізопростол (в залежності від розміру матки:
- 13–17 тижнів: 200 мкг вагінально через 6 годин (макс. чотири дози);
- 18–26 тижнів: 100 мкг вагінально (макс. чотири дози), другу дозу через 6 годин у разі потреби.
або
- евакуація за допомогою вакуумної аспірації та кюретажа при необхідності.
Профілактику антибіотиками слід почати перед хірургічною евакуацією – 200 мг доксицикліну протягом 2 год. перед процедурою або разова доза 500 мг азитроміцину протягом 2-х год.до процедури
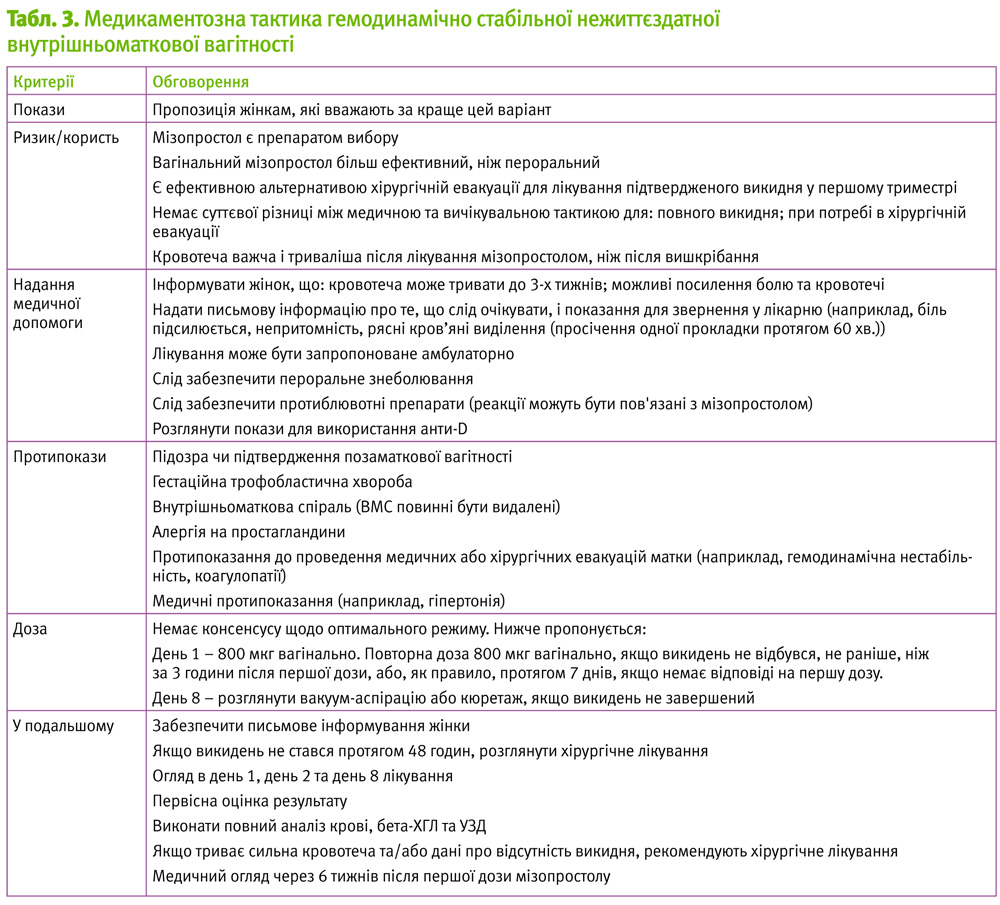
Якщо антибіотики недоступні, процедура не повинна бути затримана (табл. 3).
Протипокази до медикаментозної терапії
Абсолютні:
- позаматкова вагітність;
- недостатність надниркових залоз;
- тривале лікування глюкокортикоїдами;
- гемоглобінопатії або антикоагулянтна терапія;
- порфірія;
- мітральний стеноз;
- глаукома;
- нестероїдні протизапальні препарати протягом попередніх 48 годин;
- нестабільна гемодинаміка або шок;
- ознаки інфекції та/або сепсис;
- підозра на міхуровий занесок на УЗД.
Відносні:
- гіпертензія (АТ> 140/90);
- важка астма

Потенційні побічні ефекти
Побічні ефекти прийому мізопростолу: біль в животі, нудота, метеоризм, головний біль, розлад шлунку, блювота та закреп.
Вакуум-аспірація і медикаментозний метод не погіршують прогноз майбутньої вагітності в порівнянні з вичікувальною тактикою (табл. 4).
Рекомендована анти-D резус профілактика у дозі 250 МО (50 мкг) для всіх резус-негативних жінок, у яких були хірургічні процедури при лікуванні викидня, що не відбувся.
Не пропонувати анти-D резус профілактику жінкам, які:
- отримували виключно медикаментозне лікування для термінації викидня; або
- вагітна жінка мала повний викидень; або
- вагітна жінка мала вагітність невідомої локалізації.
Не використовувати тест Kleihauer для кількісної оцінки кровотечі матері та плода. Анти-DIg не використовується при самовільному викидні, у 12+0 тиж., до інструментальної або медичної евакуації матки. 250 МО анти-DIg зазвичай призначається протягом 72 год. після події.
Контрольне УЗД проводять не раніше 10–14 діб після евакуації плодового яйця. Більш раннє обстеження призводить до необґрунтованого збільшення частоти вишкрябання стінок порожнини матки.
Якщо немає можливості зробити УЗД, виконують тест на b-ХГЛ у сироватці крові та опитують пацієнтку про характер виділень з піхви. Рішення про «прикриття» евакуації порожнини матки протимікробними засобами приймають індивідуально з урахуванням підвищеного ризику інфекційних ускладнень, пов'язаного з присутністю в товщі стінки матки некротизуючих тканин плодового яйця.
Обстеження після викидня, що не відбувся
- Ускладнення зустрічаються рідко і, як правило, пов'язані з процесом евакуації матки.
- Затримка часток аномальних продуктів запліднення може статися і після медикаментозної або хірургічної евакуації, але більш поширене після медикаментозного лікування.
- Якщо загибель плода відбувається протягом більше 4 тижнів, рівень фібриногену може зменшитися та (рідко) може стати чинником виникнення кровотечі.
- У 80–90% пацієнтів, що мали один мимовільний аборт, згодом, при наступній вагітності, не відзначається гестаційної патології.
- Для пацієнтів з 2 або більше викиднями, що не відбулися, та інших втрат вагітності у ранніх термінах, прогноз дещо гірший. Проводиться пошук антифосфоліпідного синдрому та тромбофілічних розладів і/або хромосомне каріотипування.


коментарів