«Здоровье женщины –это здоровье нации в целом»
Интерес к метаболическому синдрому в последние годы резко возрос со стороны различных специалистов, в том числе, и акушеров-гинекологов. Актуальность метаболического синдрома в современной медицине вызвана, прежде всего, его большим медико-социальным значением. Это обусловлено высокой распространенностью метаболического синдрома в общей популяции (до 14–24%).
Ведение беременности, родов и послеродового периода у женщин с метаболическим синдромом до настоящего времени продолжает оставаться одним из актуальных вопросов акушерства. Это связано, в первую очередь, с тем, что указанная патология является причиной развития таких осложнений беременности как преэклампсия различной степени тяжести, преждевременная отслойка нормально расположенной плаценты, аномалии сократительной деятельности, послеродовые кровотечения. Данные осложнения значительно увеличивают материнскую и перинатальную заболеваемость и смертность.
Эксперты Всемирной организации здравоохранения (ВОЗ) считают метаболический синдром (синдром Х, метаболические нарушения в организме, предшествующие ожирению) «глобальной эпидемией» современности. Эксперты предполагают, что к 2025 году число страдающих этим синдромом во всем мире составит 300 млн. человек, определяя данный синдром как новую пандемию ХХI века.
Метаболический синдром (МС) – это комплекс взаимосвязанных и взаимообусловленных гемодинамических и метаболических расстройств, развивающихся в условиях инсулинорезистентности (ИР) и гиперинсулинемии (ГИ).
Метаболический синдром является типичным проявлением «болезни цивилизации», в течение нескольких веков он изучался различными авторами и получил разные названия: синдром «благополучного состояния» (H. Mehnert, 1964); синдром Х (G. Reaven, 1989); смертельный квартет (N. Kaplan, 1989); синдром инсулинорезистентности (R. DeFronzo, 1991); смертельный секстет (G. Enzi, 1994); метаболическая петля (Е. Г. Волкова, 1998); метаболический синдром X (Ю. В. Зимин, 1998).
Этиология и патогенез метаболического синдрома
Этиология и патогенез МС изучены довольно хорошо. Однако единого мнения относительно главного патогенетического фактора МС, обусловливающего все остальные проявления, до сих пор нет. Большинство исследователей считают, что ведущая роль в патогенезе метаболического синдрома принадлежит инсулинорезистентности и вызванной ею компенсаторной гиперинсулинемией, которая: снижает чувствительность инсулиновых рецепторов, вследствие чего глюкоза и жиры, поступающие с пищей, депонируются жировой тканью; подавляет распад жиров, что способствует прогрессированию висцерального ожирения; истощает секреторный аппарат бета-клеток поджелудочной железы, что приводит к нарушению толерантности к глюкозе, а впоследствии и к сахарному диабету типа 2. При висцеральном ожирении адипоциты висцеральной жировой ткани секретируют свободные жирные кислоты непосредственно в воротную вену печени, что в сочетании с повышением уровня глюкозы в крови приводит к увеличению синтеза в печени триглицеридов, ЛПОНП, ЛПНП. Снижается также содержание ЛПВП.
При физиологически протекающей беременности происходит постепенное увеличение резистентности к инсулину, что выражается в снижении действия инсулина на 50% в конце III триместра. Чтобы компенсировать это состояние, усиливается функция b-клеток в три раза по сравнению с реакцией b-клеток на то же количество глюкозы до беременности. Наличие физиологической ИР и сохранность компенсаторных механизмов обеспечивает нормальное развитие беременности. У женщин с наследственной неполноценностью инсулярного аппарата или при существовании каких-либо сбоев механизмов компенсации увеличение степени ИР будет способствовать переходу физиологической ИР в патологическую, приводя как к развитию осложнений беременности, так и к различным метаболическим нарушениям.
Одним из главных признаков метаболического синдрома (МС) является ожирение. В настоящее время ожирение рассматривается в качестве одной из основных причин нарушений функции репродуктивной системы у женщин.
Частота распространенности ожирения среди беременных составляет 15–38%. Среди беременных с ожирением большинство – в возрасте 21–25 лет (30–32% случаев) и 26–30 лет (26–28% случаев). Однако, число беременных с ожирением в старших возрастных группах также достаточно велико и может достигать 37–40%. Первородящие женщины составляют 34,1–36% случаев, повторнородящие — 52–64% случаев.
Метаболический синдром, как правило, развивается постепенно и длительное время не имеет явной клинической симптоматики. Очень важно диагностировать МС на ранних этапах его формирования.
Основные симптомы и проявления МС:
- абдоминально-висцеральное ожирение;
- ИР и гиперинсулинемия;
- дислипидемия (липидная триада);
- артериальная гипертензия;
- нарушение толерантности к глюкозе/сахарный диабет 2-го типа;
- ранний атеросклероз/ишемическая болезнь сердца (ИБС);
- нарушения гемостаза;
- гиперурикемия и подагра;
- микроальбуминурия;
- гиперандрогения.
Диагностика МС
1. Семейный анамнез (наличие наследственной склонности к ожирению, сахарному диабету, артериальной гипертензии, ишемической болезни сердца, подагре).
2. Социальный анамнез (нарушение здорового образа жизни; алиментарные привычки в виде склонности к перееданию, нарушение режима приема пищи с перемещением основного суточного рациона на позднее вечернее время; профессия и должность; стрессовые ситуации).
3. Акушерский и гинекологический анамнез (масса тела при рождении — прежде всего, дефицит массы тела при рождении с дальнейшим опережающим приростом массы тела и ранним развитием ожирения, а также избыточная масса тела при рождении; нарушения менструального цикла — преимущественно олигоопсоменорея, на фоне которой возможно развитие маточных кровотечений; раннее или своевременное менархе, преждевременное адренархе; первичное или вторичное бесплодие, невынашивание беременности, гестационный сахарный диабет, гестационная артериальная гипертензия).
4. Выявление симптомов избытка выработки тестостерона у женщин (гирсутизм, вульгарные угри, андрогенное лобно-височное облысение, себорея).
5. Выявление клинических признаков инсулинорезистентности (нарушения дыхания во время сна — храп и обструктивное сонное апноэ; нигроидный акантоз — папиллярно-пигментная дистрофия кожи в виде локализованных участков бурой гиперпигментации в области кожных складок, чаще шеи и подмышечных впадин; булимия; тромботические осложнения).
6. Антропометрические данные (рост, вес тела, значение индекса массы тела, отношение «талия–бедро»). Для выявления отложения жира в абдоминальной области следует определять:
- отношение размера талии (ОТ) к размеру бедра (ОБ). Окружность талии измеряют в сантиметрах на уровне середины расстояния между гребнем подвздошной кости и реберной дугой по средней подмышечной линии; окружность бедер — на уровне больших вертелов бедренных костей; абдоминальное ожирение констатируют при величине ОТ/ОБ, равном или большем, чем 0,9 для мужчин, и больше чем 0,85 для женщин;
- окружность талии (в см). В Рекомендациях европейских экспертов (1998 г.) рекомендуется считать показателем абдоминального ожирения окружность талии, превышающую 80 см для женщин. Окружность талии для мужчин свыше 102 см и для женщин свыше 88 см рекомендуется считать прямым указанием на необходимость снижения массы тела с применением всех возможных средств, включая медикаментозные.
- Выявление артериальной гипертензии — измерение и суточное мониторирование уровня артериального давления (АД). АД измеряют в положении сидя через 5–10 мин после последней физической нагрузки. Если систолическое АД (САД) превышает 140 мм рт. ст. и диастолическое давление АД (ДАД) выше 90 мм рт. ст., следует повторить определение давления с пятиминутным интервалом. Если двукратное определение АД выявило даже пограничную артериальную гипертензию (уровень САД равен 140–160 мм рт. ст. и уровень ДАД равен 90–95 мм рт. ст.), следует поставить вопрос о диагностике других компонентов метаболического синдрома.
7. Определение липидного спектра сыворотки крови для выявления атерогенной дислипидемии. Следует определять концентрацию в сыворотке крови общего холестерина, триглицеридов, холестерина, ЛПВП, ЛПНП, ЛПОНП с расчетом коэффициента атерогенности.
8. Определение уровня глюкозы в плазме крови натощак.
9. Определение уровня инсулина в плазме крови натощак.
10. Проведение исследования на толерантность к глюкозе с одновременным исследованием уровня инсулина в плазме крови. О наличии инсулинорезистентности может свидетельствовать выявление сахарного диабета второго типа или нарушений толерантности к глюкозе.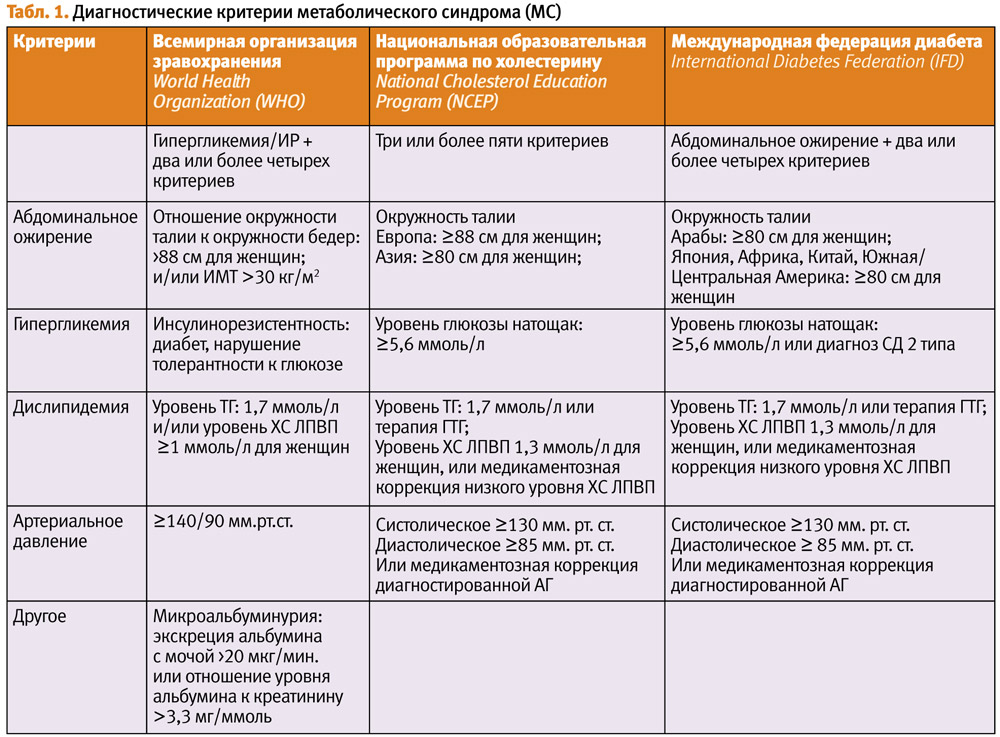
Ведение беременных с ожирением на догоспитальном этапе
Всем женщинам детородного возраста следует рекомендовать стабилизировать их вес до беременности. Внимательно к этому вопросу следует относится на этапе планирования семьи, доктор должен проинформировать женщину детородного возраста с ИМТ ≥30 о рисках, связанных с ожирением во время беременности и родов. Данным пациенткам необходима помощь в снижении веса до наступления беременности.
По сравнению с женщинами с нормальным весом до беременности, женщины с ожирением подвергаются повышенному риску выкидыша, гестационного диабета, преэклампсии, венозной тромбоэмболии, индуцированных родов, кесарева сечения, послеродовой инфекции, и они имеют меньше шансов инициировать или поддерживать грудное вскармливание (Табл. 2).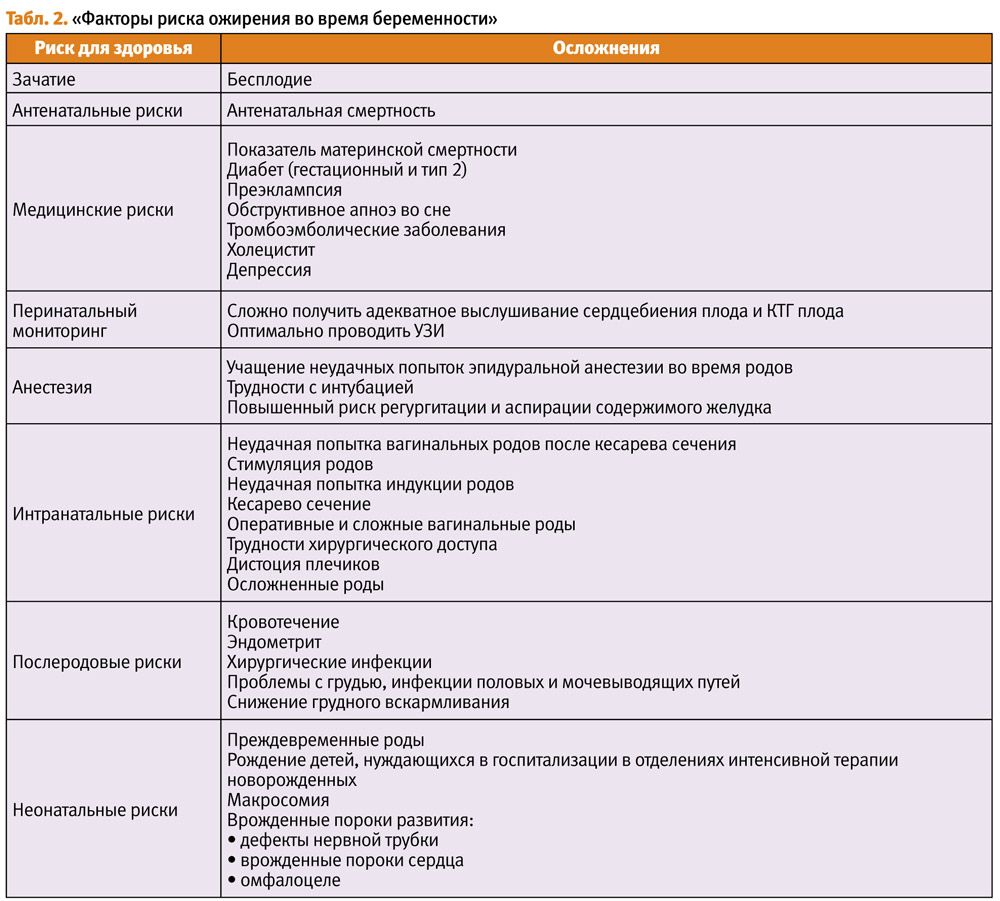
Дети, матери которых страдали ожирением, подвергаются повышенному риску мертворождения, врожденных аномалий, недоношенности, макросомии и неонатальной смертности.
При рождении детей у женщин с ожирением, у которых снизился вес, было показано, что риск развития гестационного сахарного диабета (ГСД) значительно снизился. При когортном исследовании, включившем 4102 женщины, не страдающих диабетом, но имеющих ожирение, было выяснено, что снижение веса не менее чем на 4,5 кг до их первой беременности снижает риск развития ГСД до 40%.
Хотя было высказано предположение, что некоторые потери веса в течение первого триместра беременности могут увеличить риск развития дефектов нервной трубки плода, потеря веса до беременности не влияет на этот риск.
По рекомендациям NICE guidance, женщинам с ИМТ ≥30, желающим стать матерью, необходимо рекомендовать прием 5 мг фолиевой кислоты ежедневно, начиная, по крайней мере, за один месяц до зачатия и продолжать прием препарата в течение первого триместра беременности. В общей популяции женщин дефицит фолиевой кислоты связан с эмбриональными врожденными пороками развития. Прием фолиевой кислоты до зачатия снижает риск развития врожденных пороков нервной трубки.
Медицинские работники должны особенно тщательно консультировать женщин с ИМТ ≥30 и объяснять необходимость приема 10 мкг витамина D в виде пищевой добавки ежедневно во время беременности и кормления грудью. До беременности ИМТ обратно пропорционально связан с концентрацией сывороточного витамина D. Беременные женщины и женщины с ожирением (ИМТ ≥30) подвергаются повышенному риску дефицита витамина D по сравнению с женщинами, у которых ИМТ <25. Уровни содержания витамина D в сыворотке крови у детей, рожденных женщинами с ожирением, также оказались ниже, чем у детей, рожденных от здоровых женщин. Основной синтез витамина D осуществляется при инсоляции кожи. Тем не менее, в Великобритании инсоляция солнечным светом соответствующих длин волн, особенно в зимний период, ограничена. Недавнее исследование в Великобритании показало, что примерно четверть британских женщин в возрасте 19–24 года и каждая шестая в возрасте 25–34 года подвергаются риску дефицита витамина D. Воздействие солнечного света на кожу женщины не всегда может быть достаточным для достижения оптимального уровня витамина D, необходимого для беременности. Поэтому рекомендован пероральный прием витамина D 10 мкг ежедневно для всех беременных и кормящих женщин.
Основные подходы в лечению МС
Терапевтические мероприятия при лечении пациенток с МС должны быть направлены на основные звенья патогенеза данного синдрома.
Учитывая, что в основе патогенеза метаболического синдрома лежит инсулинорезистентность и гиперинсулинемия, методы его терапии должны быть направлены на повышение чувствительности тканей к инсулину. С одной стороны, известно, что при нормализации режима, физических тренировках, снижении массы тела происходит увеличение чувствительности тканей к инсулину, снижение или нормализация артериального давления и улучшение липидных показателей крови. С другой стороны, необходимо учитывать, что помимо ИР и ГИ, данный синдром включает ожирение, нарушение углеводного обмена, дислипидемию, АГ, нарушения в системе гемостаза. При этом данный симптомокомплекс может протекать с преобладанием нарушения того или иного вида обмена, что в конечном счете определяет приоритетные направления его терапии в том или ином случае.
Немедикаментозные методы и мероприятия, направленные на снижение массы тела:
- диета низкой энергетической ценности;
- повышение физической активности.
Медикаментозные методы лечения основных проявлений МС:
- сахароснижающие препараты;
- гипотензивная терапия;
- гиполипидемическая терапия;
- цитопротекторная терапия;
- контроль свертываемости и фибринолитической активности крови;
- коррекция витамино-минерального дисбаланса.
Приоритет в лечении МС принадлежит немедикаментозным мероприятиям, которые направлены на формирование так называемого «здорового образа жизни». Это снижение массы тела, изменение стереотипов питания, отказ от вредных привычек, таких как курение и злоупотребление алкоголем, повышение физической активности.
Как уже говорилось выше, метаболический синдром является фактором риска развития серьезных осложнений беременности, родов и послеродового периода, поэтому следует уделить пристальное внимание его профилактике и лечению.


коментарів